محاسبات مولاریته

چگونه شیمی را بیاموزیم؟
آذر ۲۶, ۱۳۹۶
تفاوت بین مولاریته و مولالیته
دی ۳, ۱۳۹۶- kian kiani
- kiandroid.ir
- kimical.ir
- آمادگی کنکور شیمی
- آموزش شیمی
- اپلیکیشن شیمی
- اپلیکیشن محاسبه گر شیمی
- اپلیکیشن محلول ها
- اپلیکیشن های شیمی
- پرسش و پاسخ محلول ها
- تست شیمی
- تست های شیمی
- تعریف مولاریته
- تقویتی شیمی
- تمرین های اضافی شیمی
- حا مسائل شیمی یازدهم
- حل تمرین های شیمی دهم
- حل تمرین های شیمی یازدهم
- حل مسائل شیمی دهم
- درس شیمی
- سایت شیمی
- سایت های مفید شیمی
- سدیم پیروات
- سوالات کنکور شیمی
- شیمی
- شیمی تجزیه
- شیمی دانشگاهی
- صنایع شیمی
- صنایع شیمیایی
- صنعت شیمی
- غلظت محلول ها
- کنکور شیمی
- کیان دروید
- کیمیکال
- محاسبات محلول ها
- محاسبات مولاریته
- مولار
- نکات کنکوری شیمی
- نکته های کنکوری شیمی
- نمونه تمرین های شیمی
- نمونه مسائل شیمی شیمی پیش دانشگاهی
- وب سایت شیمی
- وبسایت های مفید شیمی
تعریف مولاریته: تعداد مول های حل شده در یک لیتر محلول
( اگر هنوز با مفهوم “مول” و “مولار”آشنا نیستید پیش از مطالعه این پست، مکعب مول و مکعب مولاریته را بخوانید)
پرسش و پاسخ محلول ها:
پرسش ۱- در محلولی به حجم ۰/۷۵۰ لیتر ۹۰ گرم اتانول حل شده وجود دارد. غلظت مولی این محلول را حساب کنید.
حل:
۱- پرسش غلظت مولی را می خواهد که تعریف آن تعداد مول های حل شده در یک لیتر محلول می باشد.
۲- جرم اتانول را با استفاده از جرم های اتمی در جدول تناوبی به مول تبدیل می کنیم که برابر ۴۶/۱ گرم بر مول می شود.
۳- اکنون با استفاده از فرمول مولاریته آن را حساب می کنیم.

پرسش ۲- اگر غلظت NaCl برابر ۰/۳۶۴ مولار باشد چند گرم از این نمک در ۱۵۲ میلی لیتر محلول وجود دارد؟
حل:
۱- سوال جرم نمک را می خواهد.
۲- داده ی مسئله مولار(مول بر لیتر) است و این به این معنی است که ۰/۳۶۴ مول از این ماده در یک لیتر حل شده
۳- چون داده بر حسب جرم(گرم) است باید جرم مولی نمک (NaCl) را حساب کنیم که برابر ۵۸/۵ می شود.
۴- در سوال حجم بر حسب میلی لیتر که باید آن را به لیتر تبدیل و سپس استفاده کنیم؟

پرسش ۳- چند گرم دکسترز در ۳۲۵ میلی لیتر محلول ۲۵۸ مولار حل شده است؟
حل:
۱- سوال درباره جرم می پرسد پس باید مقدار گرم را حساب کنیم
۲- داده برابر ۰/۲۵۸ مولار است یعنی ۰/۲۵۸ مول بر لیتر
۳- چون صورت مسئله جرم را داده پس باید جرم مولی دکسترز را بدانیم، با استفاده از جدول تناوبی ۱۸۰ گرم بر مول می شود.
۴- صورت مسئله حجم را بر حسب میلی لیتر داده که باید آن را به لیتر تبدیل کنیم که می شود ۰/۳۲۵ لیتر
اکنون با استفاده از داده ها مسئله را حل می کنیم.
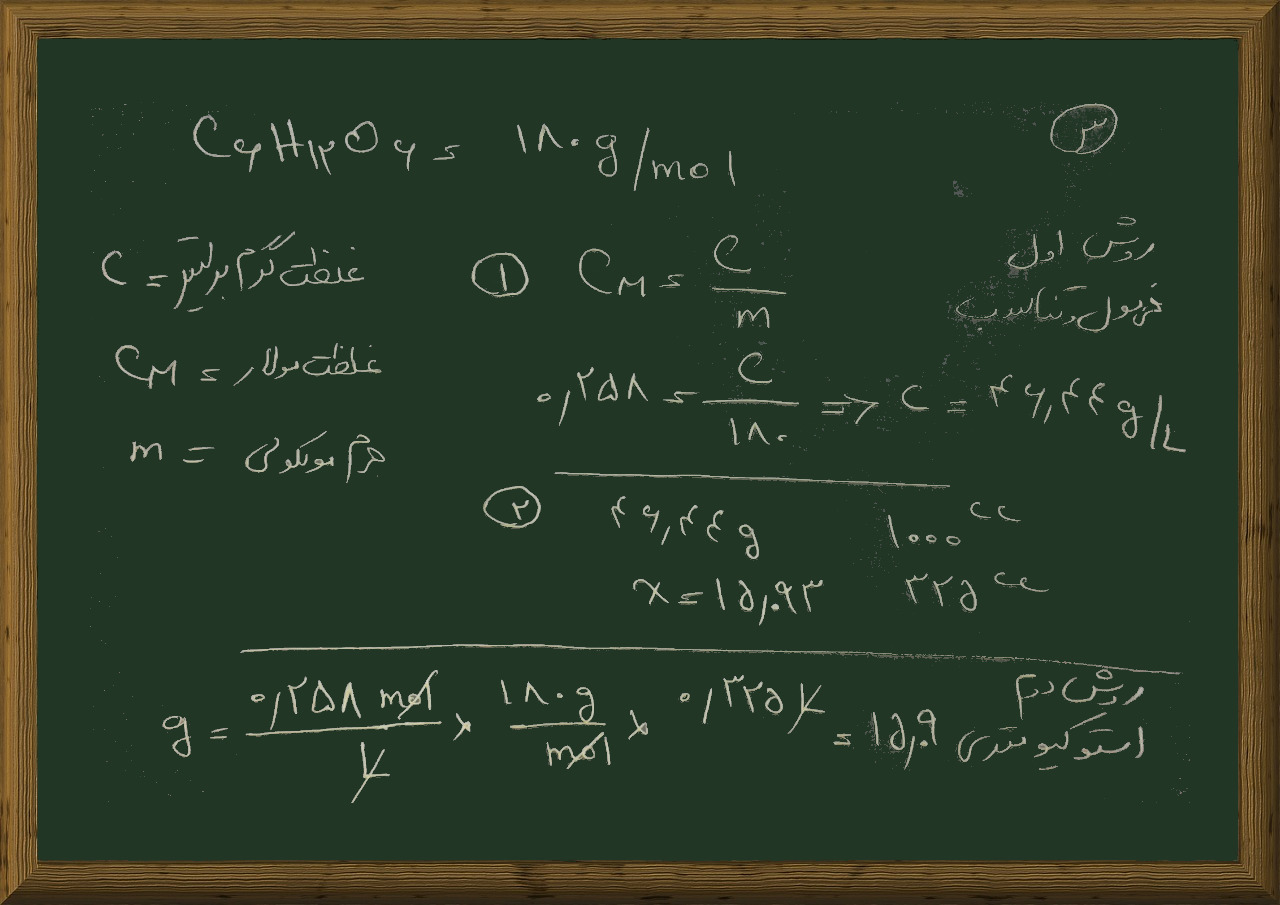
پرسش ۴- مقدار ۹۸ گرم سولفوریک اسید را با آب به چه حجمی برسانیم تا محلول نیم مولار داشته باشیم؟
حل:
۱- سوال حجم محلول را می خواهد که باید بر حسب لیتر یا میلی لیتر به دست آوریم
۲- غلظت محلول نیم مولار یعنی نیم مول بر لیتر می باشد.
۳- چون سوال شامل جرم است باید جرم مولکولی سولفوریک اسید را بدانیم که با استفاده از جدول تناوبی می شود ۹۸ گرم بر مول
اکنون با استفاده از داده ها مسئله را حل می کنیم.

پرسش ۵- مولاریته ی محلولی از سدیم کربنات Na2CO3 شامل ۵۳ گرم ماده ی حل شده در ۲۱۵ میلی لیتر محلول چقدر است؟
حل:
۱- پرسش مولاریته را می خواهد
۲- جرم را به مول تبدیل کنید برای این منظور باید جرم مولی سدیم کربنات را با استفاده از جدول تناوبی پیدا کنیم که می شود ۱۰۶ گرم بر مول می شود
۳- برای حل مولاریته به حجم هم احتیاج داریم که در صورت مسئله ۲۱۵ میلی لیتر یا ۰/۲۱۵ ذکر شده
اکنون از این داده ها در حل مسئله استفاده می کنیم
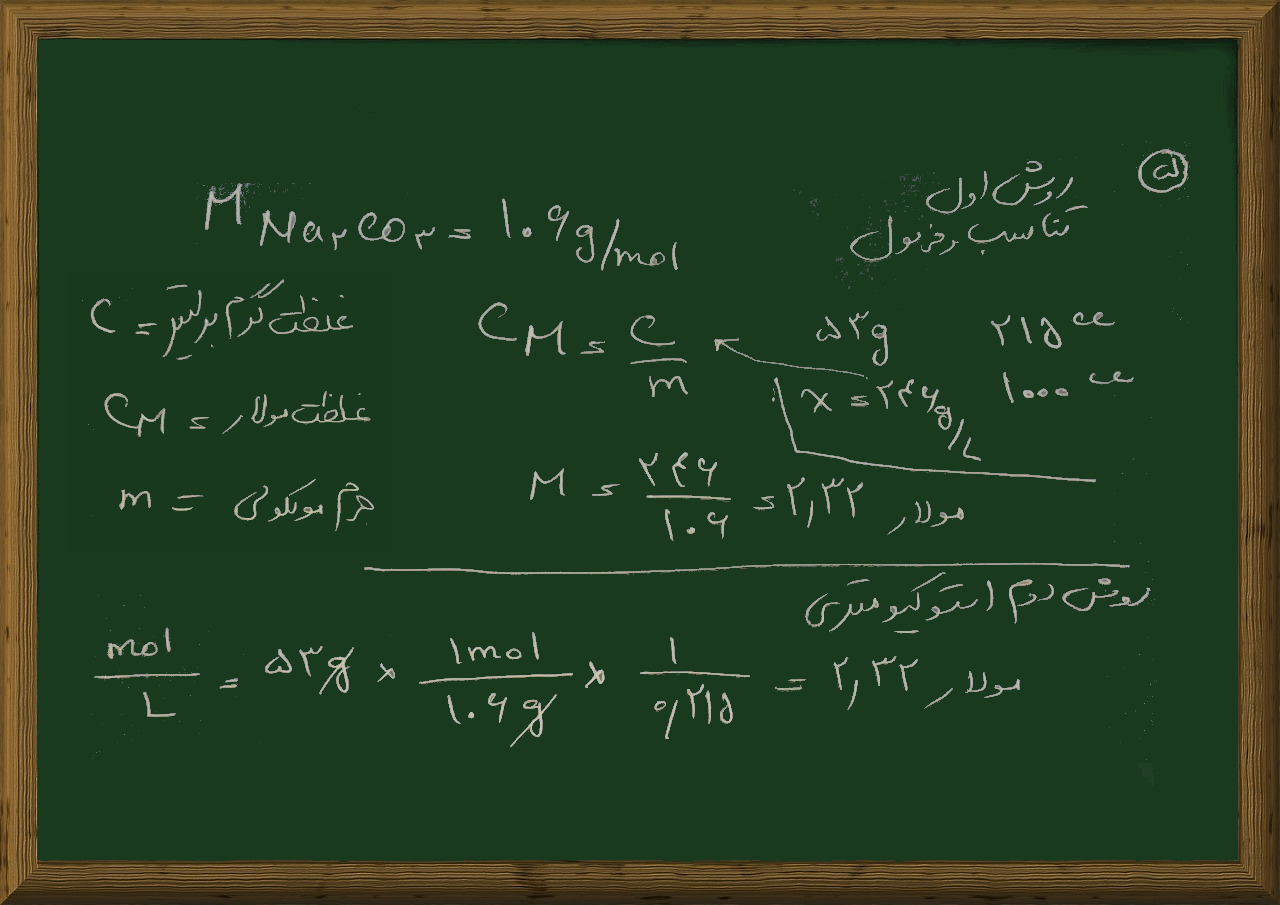
پرسش ۶- مولاریته ی محلول نیتریک اسیدی را حساب کنید که شامل ۱۲/۶ گرم در ۵ لیتر محلول است؟
حل:
۱- پرسش مولاریته را می خواهد.
۲- جرم را به مول تبدیل کنید برای این منظور باید جرم مولی نیتریک اسید را با استفاده از جدول تناوبی پیدا کنیم که می شود ۶۳ گرم بر مول می شود
۳- برای حل مولاریته به حجم هم احتیاج داریم که در صورت مسئله ۵ لیتر ذکر شده
اکنون از این داده ها در حل مسئله استفاده می کنیم
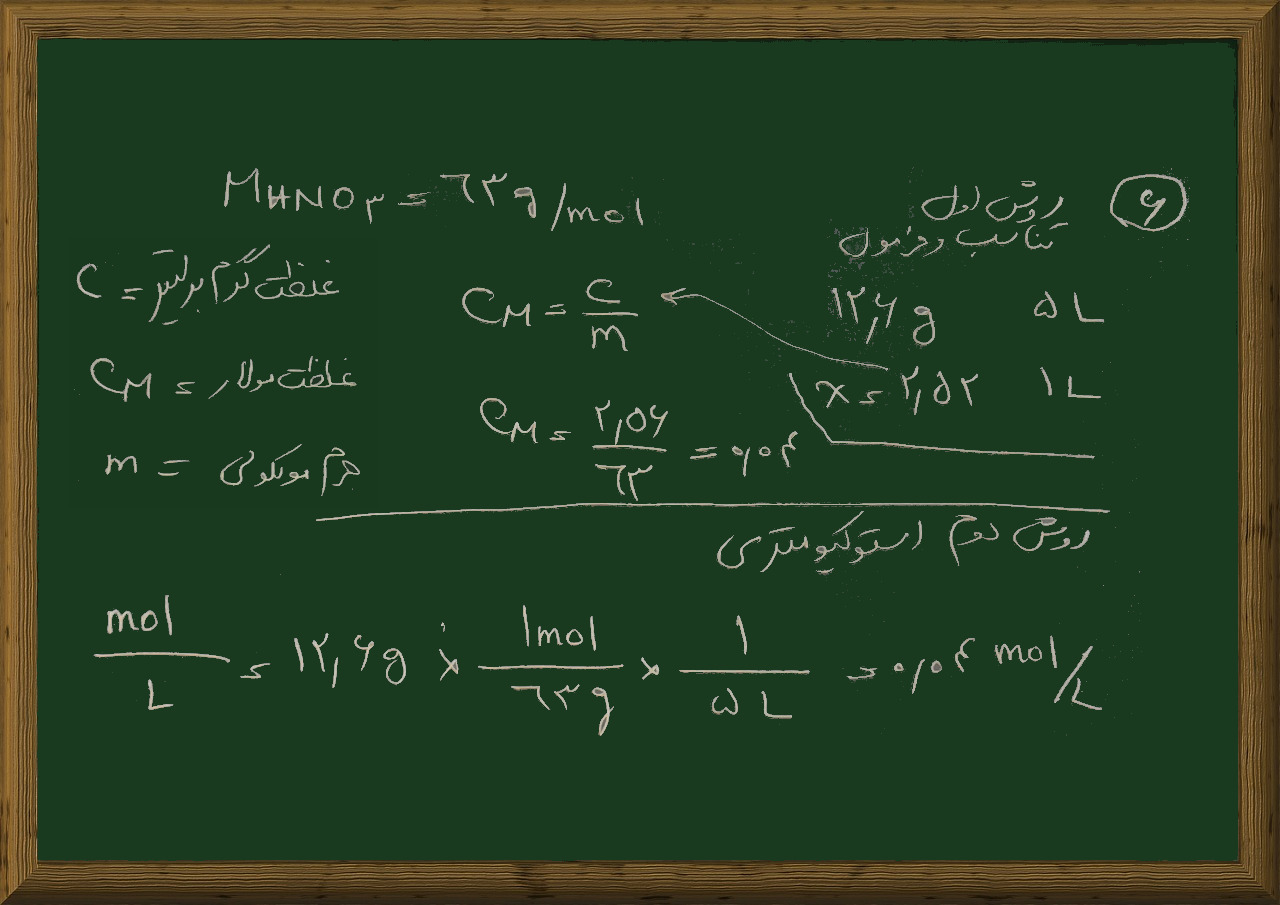
پرسش ۷- چند گرم مس(II) نیترات در ۵۰ میلی لیتر محلول ۰/۰۰۴۵۵ مولار وجود دارد؟
حل:
۱- پرسش جرم را می خواهد
۲- غلظت مولار(مول بر لیتر) به ما داده شده
۳- چون مسئله شامل جرم است باید جرم مولکولی را پیدا کنیم که با استفاده از جدول تناوبی می شود: ۱۸۷/۶ گرم بر مول
۴- از آنجایی که حجم بر حسب میلی لیتر داده شده باید آن را به لیتر تبدیل کنیم.

پرسش ۸- مولاریته محلول سولفوریک اسید ۹۵٪ با چگالی ۱/۸ گرم بر سانتی متر مکعب را به دست آورید؟
برای تهیه ی ۵۰۰ میلی لیتر سولفوریک اسید ۲ مولار چند سی سی از این اسید را باید به حجم ۵۰۰ میلی لیتر برسانیم؟
حل:
۱- این مسئله ابتدا غلظت اسید غلیظ را می خواهد و سپس از ما می خواهد حساب کنیم چقدر از این اسید غلیظ را باید استفاده کنیم تا اسید ۲ نرمال داشته باشیم
۲- جرم مولکولی سولفوریک اسید را با استفاده از جدول تناوبی پیدا می کنیم که می شود ۹۸ گرم بر مول
۳- با توجه با داشتن درصد و چگالی اسید از فرمول مناسب استفاده می کنیم
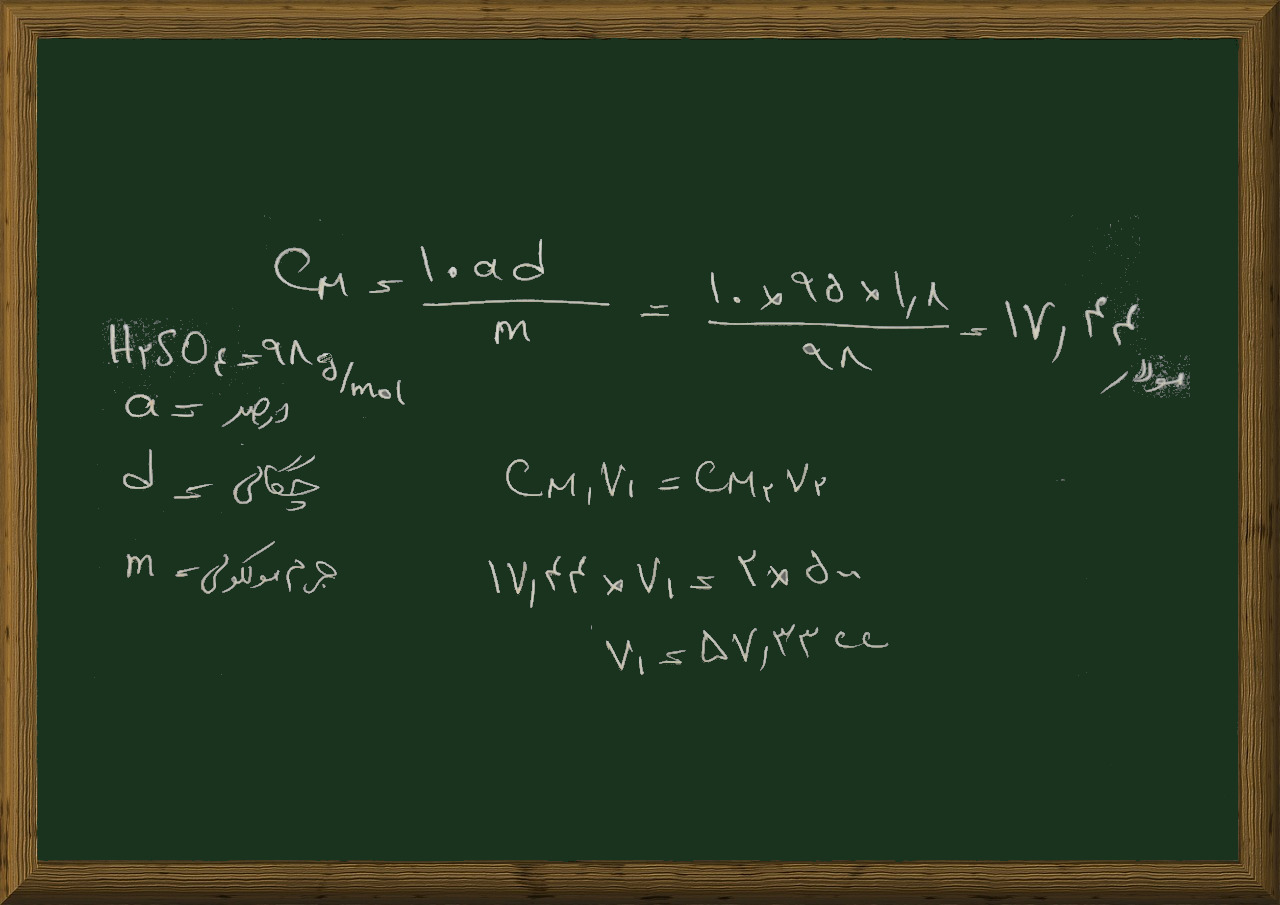
پرسش ۹- چندمیلی لیتر از هیدروکلریک HCl هشت دهم ۰/۸ مولار برای خنثی کردن کامل ۲۰ گرم کلسیم کربنات لازم است؟
حل:
۱- ابتدا معادله واکنش موازنه شده را بنویسید:
CaCO3 + 2HCl → CaCl2 +CO2 + H2O
طبق معادله ی بالا هر مول کلسیم کربنات با دو مول هیدروکلریک اسید واکنش می دهد
جرم مولکولی کلسیم کربنات ۱۰۰ گرم بر مول و جرم مولکولی HCl برابر ۳۶/۵ گرم بر مول پس طبق معادله واکنش موازنه شده هر ۱۰۰ گرم کلسیم کزبنات با ۲×۳۶/۵ = ۷۳ گرم HCl واکنش می دهد.
۲- با استفاده از فرمول مولاریته غلظت گرم بر لیتر هیدروکلریک اسید را به دست می آوریم
پرسش ۱۰- چطور میتوانم محلول دو میکرو مول بر میلی لیتر سدیم پیروات درست کنم؟
حل: ابتدا باید میکرومول بر میلی لیتر را به گرم بر لیتر تبدیل کنید:
اکنون در یک بالن ژوژه یک لیتری تا نیمه آب مقطر میریزیم و سپس ۰/۲۲ گرم سدیم پیروات را در آن حل می کنیم و با آب مقطر به حجم می رسانیم.
مطالب مرتبط با این پست:
محاسبات پی پی ام
محاسبات نرمالیته
تفاوت مولاریته و مولالیته
نکات کنکوری شیمی
تبدیل پی پی ام و مولار به همدیگر
اپلیکیشن های مرتبط با این درس:
اپلیکیشن محلول ها
اپلیکیشن محاسبه گر شیمی
برای سهولت در بازبینی وب سایت شیمی کیمیکال و ده ها وب سایت شیمی ایرانی و خارجی دیگر و شبکه های اجتماعی مرتبط و همچنین سهولت در به اشتراک گذاری مطالب آن ها اپلیکیشن رایگان کیمیکال پلاس را نصب کنید.

https://sites.prairiesouth.ca/legacy/chemistry/chem30/4_solutions/practice/a2_2.htm







76 Comments
خیلی خوب متوجه شدم واقعا ممنون
خوب وقتی بگه چندمیلی لیتر ازhcl 0/8مولار برای خنثی کردن کامل ۲۰ گرم کلسیم کربنات لازم است؟؟؟
پاسخ شما به همین مجموعه اضافه شد
پرسش ۹ را ببینید
خیلی ممنون که جواب دادید میشه بگید چه جوری میشه واکنش هارو تویه مسایل است وکیومتری نوشت من داوطلب کنکورارشدبیوشیمیم اخرتیرکنکوردارم خواهش میکنم راهنماییم کنید
سلام ببخشید میشه راه حل این مساله رو بفرستید؟
مولاریته یک محلول۰/۵مولار ساکارز در آب چقدر است ؟
چگالی محلول ۱/۰۶۴g/ ml و وزن مولکولی برابر ۳۴۲/۳ است
خیلی ازتون ممنونم که جواب دادید خواهش میکنم میشه برای این که معادله واکنش های رو تویه مسایل استوکیومتری نوشت راهنمایی کنید خواهش میکنم
ممنون که جواب دادید میشه توضیح بدید که چه جوری معادله واکنش هارو توی مسایل استوکیومتری نوشت ؟خواهش میکنم ج بدید
درود
لینک زیر را ببینید
http://kimical.ir/cr/
سلام و عرض ادب. ممنون از وبسایت بسیار خوبتون.
ممنون میشم سوالم را پاسخگو باشید:
هر میلی لیتر HCL ١ نرمال برابر با چند میلیگرم سدیم استات میباشد؟ وزن مولکولی سدیم استات: ٨٢.٠٣
سپاس
جواب پرسش شما در لینک زیر گنجانده شد(مسئله شماره شش)
http://kimical.ir/normal/
برای سهولت در بازبینی وب سایت شیمی کیمیکال و ده ها وب سایت شیمی ایرانی و خارجی دیگر و شبکه های اجتماعی مرتبط و همچنین سهولت در به اشتراک گذاری مطالب آن ها اپلیکیشن رایگان کیمیکال پلاس را نصب کنید.
سلام و با تشکر از سایت خوبتون
من میخوام محلول kcl درست کنم با غلظت ۶۰ میلی مولار و بعد در یک محفظه به حجم ۵۰ میلی لیتر اضافه اش کنم
ممنون میشم کمکم کنید
درود
محلول شما باید ۴/۴۷ گرم بر لیتر باشد
برای ۵۰ میلی لیتر می شود ۰/۲۲۳۵ گرم
یعنی باید یک بالن ژوژه ی ۵۰ سی سی را بردارید سپس تا نیمه از آب مقطر پر کنید و ۰/۲۲۳۵ گرم پتاسیم کلرید را در آن حل کنید و دوباره با آب مقطر به حجم ۵۰ سی سی برسانید.
سلام لطفا میخواستم چگونگی ایجاد این فرمول رو برای محاسبات مولاریته بهم بگین سپاس
مولار=۱۰×درصدجدمی×چگالی
__________________
جرم مولی
سلام با اجازه از مطالبتون در ارائه ام استفاده میکنم
از درستکاری شما سپاس گزارم
اگرچه استفاده از مطالب کیمیکال آزاد است
فقط اگر در صورت تمایل منبع را ذکر کنید برای افزایش بازدید سایت و معرفی آن به دیگران مفید است
شاد و پیروز باشید
فوق العاده و جامع بود .سپاس
۳ مول اسید hcl با درصد خلوص ۳۷ درصد برابر با چند cc اسید است ؟
۲۱۴cc
سلام توروخدا جوابمو بدین خیلی نیاز دارم
برای فرمول تستی غلظت مولی که چگالی توش هست چگالی باید یکای گرم بر میلی لیتر باشه؟
یعنی اگه با یکای گرم بر لیتر بری اشتباهه؟
درود
گرم بر سانتی متر مکعب
سانتی متر کعب= میلی لیتر= سی سی
A sample of 1.42 g of sodium sulfphate (NaSOs) is dissolved in 100 g of water.Calculate the percent by mass of Na,SO, in this solution
سلام . ممنون میشم در مورد این سوال توضیح بدین لطفا
با عرض سلام و خسته نباشید
مطالب و مفاهیم پایه و اساسی بسیار ساده ، کامل و جامع شرح داده شده است.رشته من به شیمی ربطی ندارد ولی در بخشهایی نیاز به محلولسازی داریم.از مطالب مفید شما استفاده کردم.حتما سایت شما را به دانشجویانم معرفی خواهم کرد.با سپاس فراوان
سپاس گزارم
سلام
تعیین درصد اسید نیتریک به چه طریق می باشد.
با تشکر
درود یک روش آسان و سریع اندازه گیری چگالی هست
http://kimical.ir/sulf/
سلام وقتتون بخیر . غلظت مولار آب اکسیژنه با دانسیته g/mL 1.11 و جرم مولی ۳۴ و درصد خلوص ۳۰% وزنی حجمی ، چه قدر میشه ؟؟
ممنون میشم راهنماییم کنین . مشکلی که من دارم اینه که استادم تاکید کرده که درصد خلوص آب اکسیژنه وزنی/حجمی است ، نه حجمی حجمی . میخواستم بدونم فرقی توی محاسباتمون میکنه ؟
سلام وقتتون بخیر . ممنون از مطالب مفیدتون .
میخواستم بدونم غلظت مولار آب اکسیژنه با دانسیته ۱.۱۱ g/mL و جرم مولی ۳۴ و درصد خلوص ۳۰% وزنی حجمی ، چه مقدار میشه ؟
ممنون میشم راهنماییم کنین . مشکلی که من دارم اینه که استادم تاکید کرده که درصد خلوص از نوع وزنی/ حجمی است ، نه حجمی حجمی .
این توی محاسبات فرق داره ؟
۹.۷۹
ممنون از جوابتون . یه سوال دیگه : در فرمول
M=10ad/M ، مهمه که درصد خلوص از چه نوعی باشه ؟
منظورم اینه این فرمول فقط برای درصد خلوص های حجمی حجمی بکار میره یا برای درصد خلوصِ وزنی حجمی هم میشه ازش استفاده کرد؟
با عرض سلام
اگر بخواهم ۱.۶ میلی مول ارژنین تهیه کنم در صورتی که جرم مولی ال ارژنین ۱۷۴.۲ گرم مول می باشد چیکار باید بکنم از اینکه سریعتر جوابمو بگیرم خیلی ممنون می شم.
با سلام و وقت بخیر
چگونه می توان از سوسپانسیون مترونیدازول نیم درصد رقت ۶۴ میکروگرم بر میلی لیتر بدست اورد؟ سپاسگزارم
با سلام و عرض ادب.
هر میلی لیتر پرکلریک اسید ۰.۱ نرمال معادل چند میلیگرم گاباپنتین است؟
وزن مولکولی پرکلریک اسید: ۱۰۰.۴۶ g/mol
وزن مولکولی گاباپنتین : ۱۷۱.۲۳۷ g/mol
فرمول شیمیایی گاباپنتین: C9H17NO2
چرا تو پرسش ۲ . ۵۸/۵ در مخرج کسر نوشته شده؟
نمیتونستیم بنابه فرمول ۱۵۲/رو تو مخرج بنویسیم؟
درود
در آن فرمول m کوچک جرم مولکولی هست
سلام و عرض ادب
برا تهیه محلول ۱۰ میلی مول کلرید پتاسیم به عنوان پایه در تهیه محلول های ۳۰ درصد و ۵۰ درصد پلی اتیلن گلیکول چه باید کرد؟
با سلام من یه محلول اب و نمک دارم با درصد جرمی ۳.۵ ،
۳.۵ درصد جرمیه هست که نمک در اب من دارد ، چطور میونم درصد و غلظت مولی نمک محلول رو بدست بیارم
مولالیته محلول ۶.۷درصد اتانول در آب؟ جرم مولی اتانول ۴۶. اگر امکان داره راه حل
عکس را ذخیره کنید
سلامممنون از توضیحاتتون
به چه صورت از منحنی کالیبراسیون LOD و LOQ رو بدست بیارم
سلام میشه این سوالو هم جواب بدید درصد جرمی آمونیاک در محلول ۱۰ مولار آن با چگالی ۹۳۵/۰ هزارم چقدر است؟
اگربه ۵لیتر محلول۰/۴molسولفوریکاسید۳۰۰میلی لیترآب مقطر اضافه کنیم غلظت مولیچندmolبرLاست؟؟
سلام مرسی از مطالب مفید تون میشه بگید با مخلوط دومحلول ۹۰ و ۵۰ درصد الکل میتونیم به محلول ۷۰ درصد برسیم ؟
درود
بله به نسبت مساوی باهم مخلوط کنید
تبدیل گرم به مول چطور میشه ممنون میشم ج بدید؟
تمرین ها را بخونید یاد می گیرید
چرا فیزیک مثل آدم میاد فرمول ها رو میگه ولی کتاب درسیه شیمی هیچ فرمول نمیگه
حتما باید بریم جزوه و این بند و بساط ها رو بخونیم
دست های پنهانی دز کار هست که بچه ها چیزی یاد نگیرند
و شیمی کاربردی تر تز فیزیک هست
مثلآ فرمول سرعت در فیزیک در هیچ کارخانه ای کاربرد ندارد اما فرمول غلظت کاربرد دارد
برای خنثی کردن ۵۰۰میلی لیتر محلول باریم هیدراکسید۰/۴ مولار چند میلی متر محلول ۲۰ درصد جرمی هیدرکلرید اسید باچگالی ۱/۴مول بر گرم لازم است؟ ( مول بر گرم Hcl= 36/5)
لطفاً جواب را بنویسید
۲ میکروگرم بر میلی لیتر چند مول بر لیتر است؟
من برای تهیه محول از این ماده جامد ابتدا باید اون رو به مولار تبدیل کنم سپس بدونم چند گرم از ماده باید بردارم. ولی خیلی مقدار مولار کم میاد و ارور میده ماشین حساب چیکار کنم لطفا راهنماییم کنید
ابتدا به گرم بر لیتر تبدیل کنید( تقسیم بر هزار)
سپس از رابطه مولاریته استفاده کنید
M=C/m
M مولاریته
C گرم بر لیتر
m جرم مولکولی
سلام
محلولی دارم که شامل ۶۰ میلی لیتر H2O و ۳۰ میلی لیتر محلول ۰.۱M نیترات نیکله ۶ آبه و ۲۰میلی لیترHCl سه مولار(۳M) که در ظرف آزمایشگاهی ۱۵۰mlتهیه میشود.
ممنون میشم راهنماییم کنید چطور بایدمحلول سازی کنم مخصوصا قسمت HCl رو .با توجه به اینکه حجم هارو بهم گفتن ÷۳ کنم تا مواد کمتری مصرف کنم
از طرفیم برای قسمت Hcl بهم اعداد زیر را دادن که نمیدونم چطور بدست امده؛
۱.۷ml HCl + 5.3ml H2O
ممنون میشم در صورت امکان محاسبشو به ایمیلم بفرستید.
سلام.
مولالیته یک محلول۶/۷%(c2H5oH) در اب چقدر است؟ وزن مولکولی اتانول ۴۶
درود بر شما
لینک زیر را باز کنید . پرسش شماره ۴ را ببینید
http://kimical.ir/molality1/
ویرایش شد دوباره ببینید
[…] مرتبط با این پست: محاسبات مولاریته تفاوت مولاریته و مولالیته نکات کنکوری شیمی برای […]
سلام خسته نباشید ممنون از سایت خوبتون
اگر میشه سوال زیر رو برام حل کنید
چنانچه بدانیم دانسیته ی آب برابر است با ۱ و دانسیته ی آب نمک با غلظت ۱ مولاریته ،۱.۲می باشدو جرم مولکولی نمک ۵۸.۵ گرم است، آیا می توانیم مولالیته ی محلول ۱ مولار را محاسبه کنیم؟
درود
لطفآ مسئله حل شده در لینک زیر را ببینید
http://kimical.ir/molarmolal/
سلام ممنون استاد از مطالبتون
سوالی داشتم چطور میتونم محلول دو میکرو گرم بر میلی لیتر سدیم پیروات درست کنم؟
درود
پرسش شماره ۱۰ را بخوانید
http://kimical.ir/molarity/
سلام ممنون استاد از مطالبتون سوالی داشتم چطور میتونم محلول دو میکرو مول بر میلی لیتر سدیم پیروات درست کنم؟
درود
پرسش شماره ۱۰ را بخوانید
http://kimical.ir/molarity/
باسلام امکانش هست این فرمول رو به روش خطی اثبات کنید؟Cm=10ad/Mw
سلام و تشکر از تمام مطالب مفید شما
۱- برای ساخت ۲۵۰ سی سی محلول ۲ مولار استات ؟
تشکر
۱-مولاریته محلول ۱۲۰گرم در لیتر Naoh را بدست آورید .۲-برای تهیه ۲۰۰میلی لیتر Hclیک دهم نرمال چقدر Hclده مولار لازم است ؟۳-برای تهیه ۵۰ccیک دهم مولارچقدر سود دودهم نرمال لازم دارد
درود
درس دادیم
بخوانید ، یاد بگیرید، و خودتون حل کنید….لذتش بیشتره
با سلام
اگر در سوالی از ما میلی مول های باقی مانده رو بخوان چطوری باید حل کنیم.
سلام وقت بخیر
برای تهیه ی محلول ابی اتانول ۱۶ درصد
حجمی _ وزنی
حجمی _ حجمی
و وزنی _ وزنی باید به چه صورت اقدام کرد؟
ممنون از راهنمایی شما??
در صورتی ک غلظت دو نرمال از نیتریک اسید به حجم ۱۵ میلی لیتر با ۲۱میلی لیتر از محلول سدیم هیدروکسید درحضور معرف منل فتالین خنثی شده باشه غلظت سدیم هیدروکسید بر حس مولاریته چنده؟اینم میشه بگین؟؟
۱.۴۲ M
مولاریته و نرمالیته برای اسیدها و باز های یک ظرفیتی برابر است
سلام خسته نباشید
اگر محلولی با غلظت دو نرمال از نیتریک اسید به حجم ۱۵ میلی لیتر با ۲۱ میلی لیتر از محلول سدیم هیدروکسید درحضور معرف فنل فتالئین خنثی شده باشه .غلظت سدیم هیدروکسید بر حسب مولاریته چقد میشه!
سلام خسته نباشید
از افزودن مقداری سدیم به آب ۵۰.۴mL گاز هیدوژن(به صورت خشک و در STP)
و ۱۷۵mL محلول NaoH بدست اومده
مولاریته و مولالیته محلول NaoH چقدره؟
به چه نسبتی آب و محلول سود ۲ نرمال را مخلوط کنیم تا محلول ۰.۲۵ مولار به دست آید؟
سلام وقت بخیر لطفا اگر زحمتی نیست این سوال را جواب دهید به چه نسبتی آب و محلول سود ۲ نرمال را مخلوط کنیم تا محلول ۰.۲۵ مولار به دست آید
سلام محلول نیترات نقره ۰۱۰۲/۰ مولار رو چطور باید تهیه کنم میشه شما کمکم کنید
سلام وقتتون بخیر
برای رسیدن به غلظت مایعات و جامدات از فرمول چگالی(g/L) تقسیم بر جرم مولی(g/mol) استفاده می کنیم ؛ یکای غلظت(mol/L)است .حالا چطوری از یکاهای(g/mol)/(g/l) به یکای غلظت یعنی (mol/l)برسیم،آخه بعد از ساده شدن gباg به یکای(L/mol) می رسیم نه (mol/L)