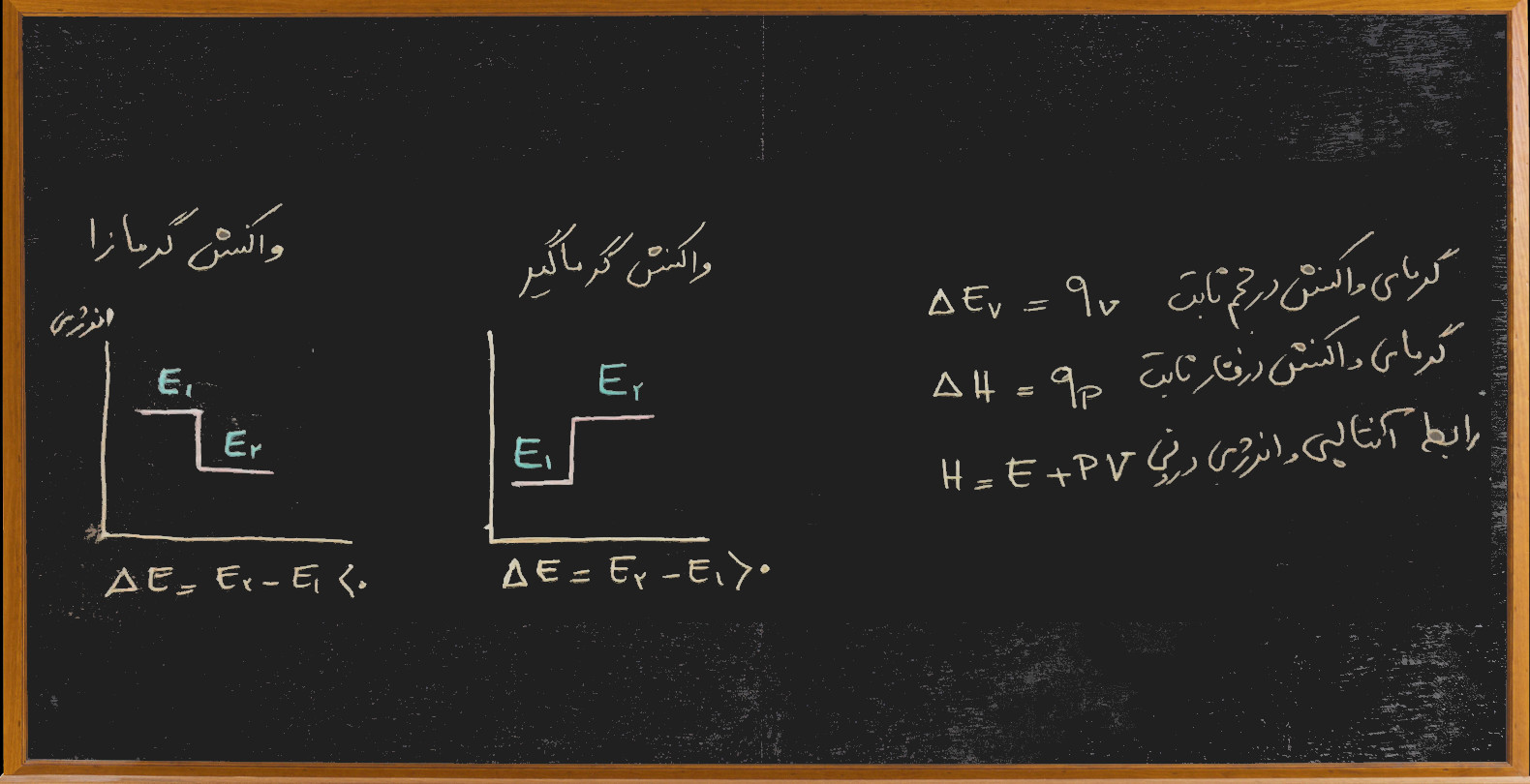گرما در واکنش های شیمی

نکات کنکوری شیمی (۷)
مهر ۶, ۱۳۹۶
سرعت واکنش های شیمیایی
مهر ۸, ۱۳۹۶از آنجایی که برای بخش های گرما، سرعت، تعادل اپلیکیشنی ننوشته ام این سه بخش را به صورت فشرده درس می دهم و سپس به نکات کنکوری آن می پردازم.
تفاوت بین گرما و دما:
گرما و دما دو واژه ای هستند که اغلب در فیزیک وشیمی مورد استفاده قرار می گیرند.دو مفهوم که به حالت فیزیکی مشابهی اشاره می کنند،اما در بسیاری جهات با یکدیگرتفاوتهاییدارند.
مردم این دو واژه را به جای هم استفاده می کنند که اشتباه است.البته وقتی درجه حرارت بالا برود گرمای جسم افزایش می یابد اما برای درک تفاوت بین این دو نیاز به درک واضحی از انرژی جسم داریم.با ما همراه باشید…
گرما:
گرما انرژی موجود در جسم است،هم انرژی پتانسیل و هم انرژی جنبشی.
انرژی پتانسیل انرژی ذخیره شده در جسم است درحالی که انرژی جنبشی انرژی در حال حرکت است.
واحد انرژی ژول (J) است.
دما (درجه حرارت) :
دما،اندازه گیری انرژی جنبشی مولکول های یک شی است.این عدد مربوط به انرژی است اما خود انرژی نیست.عددی است که با واحدهایی مانند کلوین،فارنهایت وسانتیگراد اندازه گیری می شود.
هنگامی که یک جسم گرم می شود،مولکول های آن سریع تر حرکت می کنند.مولکولها به یکدیگر برخورد می کنند که موجب تولید گرما وحرارت بیشتری می شود ودرجه حرارت جسم بالا می رود.
بخش گرما:
-گرمای یک واکنش: یک واکنش شیمیایی شامل شکستن یک سری از پیوند ها و تشکیل یک سری پیوند های جدید می باشد. شکستن پیوند گرما گیر و تشکیل پیوند گرما زا می باشد.
اگر انرژی لازم برای شکستن پیوندهای قدیمی بیشتر از انرژی حاصل از تشکیل پیوند های جدید باشد آن واکنش گرماگیر خواهد بود و اگر انرژی لازم برای شکستن پیوندهای قدیمی کمتر از انرژی حاصل از پیوندهای جدید باشد آن واکنش گرمازا یا گرماده خواهد بود.
-تعریف انرژی درونی(E): به مجموع انرژی درونی و انرژی ذخیره انرژی درونی می گویند
-تعریف انرژی پیوند: حداقل انرژی لازم برای شکستن یک پیوند یا حداقل انرژی حاصل از تشکیل یک پیوند.
-تعریف گرمای تشکیل مولی: مقدار گرمای مبادله شده برای تشکیل یک مول ماده ی مرکب از اجزای سازنده اش.
-تعریف گرمای سوختن: مقدارگرمای حاصل از سوختن یک مول ماده ی سوختنی
-تعریف گرمای انحلال: مقدارگرمای مبادله شده در اثر انحلال یک ماده ی حل شدنی در حلال
-شرایط یک واکنش خودبه خودی: ۱- گرمازایی ۲- افزایش بی نظمی(یعنی تعداد مول های گاز طرف دوم بیشتر از طرف اول باشد)
-شرایط یک واکنش دو طرفه: اگر یکی از شرایط فوق (گرمازایی و افزایش بی نظمی) موجود نباشد آن واکنش دو طرفه خواهد بود.
-روش های محاسبه گرمای یک واکنش:
برای فراگیری بهتر پیش نیازهای این بخش از شیمی عمومی اپلیکیشن از اتم تا استوکیومتری را مطالعه کنید