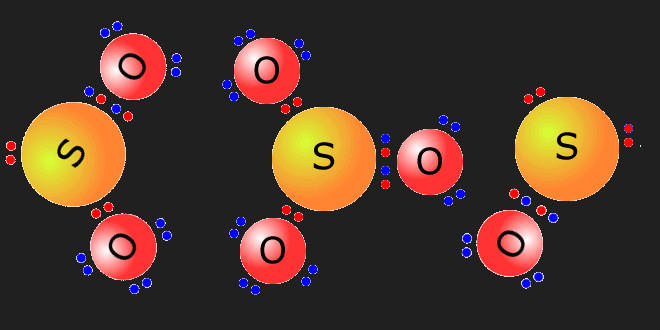
اکسیدها و اسیدهای اکسیژن دار گوگرد(۱)
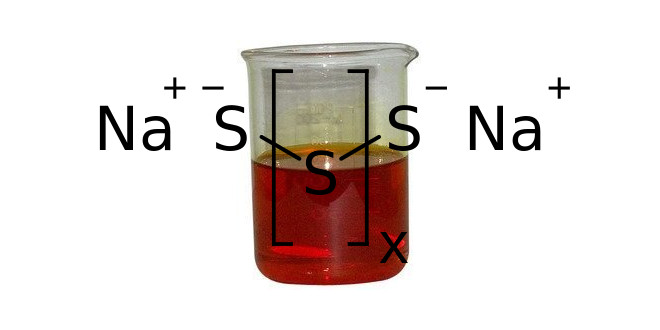
هیدروژن پلی سولفیدها یا سولفانها (Sulfanes)
بهمن ۲۳, ۱۳۹۶
آتش سوزی بوسیله آب
بهمن ۲۵, ۱۳۹۶همانطوری که می دانیم گوگرد یکی از عناصر گروه ششم جدول تناوبی عناصر می باشد و تمامی عناصر گروه ششم جدول تناوبی عناصر (باستثناء اکسیژن) با اکسیژن ترکیب شده و دو نوع اکسید بفرمول عمومی XO2 و XO3 (به ترتیب با درجات اکسایش ۴+ و ۶+) تولید می نماید که اکسیدهای مذکور اکسید اسیدی (انیدرید) هستند و با آب ترکیب و تولید اسید مینمایند طبق فرمولهای عمومی زیر:
XO2 + H2O → H2XO3 (X=+4)
XO3 + H2O → H2XO4 (X=+6)
مانند ترکیب آب با SO2 و SO3 که بترتیب اسید ارتوسولفور و اسید ارتو سولفوریک به دست می آید:
ارتوسولفورو اسید
SO2 + H2O → H2SO3 (S=+4)
ارتوسولفوریک اسید
SO3 + H2O → H2SO4 (S=+6)
بطوریکه مشاهده می شود گوگرد در دو واکنش بالا به ترتیب دارای درجه اکسیداسیون (۴) و (۶) می باشد و علاوه از اسید ارتوسولفورو و اسید ارتوسولفوریک اسیدهای متعدد دیگری از گوگرد وجود دارند که گوگرد در آنها هم دارای درجه اکسیداسیون (۴) یا (۶) می باشد و فقط از نظر تعداد مولکولهای آبی که برای ترکیب با یک مولکول SO2 یا SO3 مصرف شده است (یعنی از نظر اختلاف ئیدراتاسیون یا ) با همدیگر (یعنی اسیدهای حاصل از با همدیگر یا اسیدهای حاصل از با همدیگر) اختلاف دارند. مثلاً دی اکسید گوگرد علاوه از اینکه اسید ارتوسولفورو تولید می کند، می تواند اسید دیگری بنام اسید پیروسولفورو طبق فرمول زیر به وجود آورد:
پیروسولفورو اسید
2SO2 + H2O → H2S2O5 (S=+4)
بهمان ترتیب تری اکسید گوگرد SO3 علاوه از اینکه اسید ارتوسولفوریک تولید می کند، میتواند اسید دیگری بنام اسید پیروسولفوریک به وجود آورد که فرمول آن بقرار زیر است:
پیروسولفوریک اسید
2SO3 + H2O → H2S2O7 (S=+6)
از دو معادله بالا بر می آید که از ترکیب دو مولکول اسید ارتو با از دست دادن یک مولکول آب (یا از ترکیب یک مولکول اکسید اسیدی با یک مولکول اسید ارتو مربوطه) اسید پیرو به دست می آید به طوریکه می دانیم از اتحاد SO3 و H2SO4 (اسید سولفوریک 98%) اسید پیروسولفوریک طبق فرمول زیر به دست می آید:
پیروسولفوریک اسید
SO3 + H2SO4 → H2S2O7 (S=+6)
اسید پیروسولفوریک را اولئوم یا اسید سولفوریک دودکننده هم می نامند و علت این نامگذاری از آنجا ناشی شده است که وقتی اسید پیروسولفوریک با هوای مرطوب تماس حاصل می کند دود سفیدی متصاعد می کند که همان مه اسید سولفوریک می باشد و از ترکیب گاز SO3با بخار آب موجود در هوا تولید می شود.
علاوه از اسیدهای مذکور ممکن است از ترکیب دو اسید مختلف با از دست دادن یک مولکول آب، اسیدهای دیگری نیز حاصل شود.
همی اکسیدگوگرد S2O : همی اکسیدگوگرد گازی است که اولین بار شخصی به نام B.S.Rao آن را تهیه کرده است و برای تهیه آن گوگرد را تحت فشاری خیلی کم در اکسیژن سوزانده و گاز حاصل را در محلولی از تتراکلرید کربن CCl4 خشک (بی آب) و ۱۲- درجه سانتی گراد (یعنی سرد شده) وارد کرد و محلولی از در تتراکلرید کربن به دست آورد. محلول در تتراکلرید کربن دارای پایداری بیشتری است ولی با این وضع در اثر حرارت حتی در اثر حرارتی خفیف سریعاً طبق فرمول زیر تجزیه شده و گوگرد و می دهد:
حرارت
2S2O → 3S + SO2
همی اکسید گوگرد (خالص) در حرارت ۲۵ نیز طبق فرمول فوق تجزیه می گردد.
هر گاه همی اکسید گوگرد را به روش فوق تهیه کرده در ۷۰- درجه سانتی گراد قرار دهند به صورت جسمی جامد و به رنگ زرد و مایل به نارنجی در خواهد آمد.
همی اکسید گوگرد با محلول سود سوزان ترکیب شده و مخلوطی از سولفیت و سولفید سدیم تولید می کند طبق فرمول زیر:
S2O + 4NaOH → Na2S + Na2SO3 + H2O
منوکسید گوگرد SO: منوکسید گوگرد ترکیبی است که برای اولین بار از اثر بعضی از فلزاتی از قبیل نقره و منیزیم بر بخار کلرور تیونیل به دست آمده است طبق فرمولهای زیر:
SOCl2 + 2Ag → 2AgCl + SO
SOCl2 + Mg → MgCl2 + SO
کلرور تیونیل هم از اثر پنتاکلرید فسفر PCl5 بر SO2 طبق فرمول زیر حاصل می شود:
SO2 + PCl5 → POCl3 + SOCl2
واکنش های دیگری نیز برای تهیه SO بکار برده شده است که یکی از آنها فرمول زیر است:
SOCl2 + SnCl2 → SnCl4 + SO
در واکنش اول بجای فلز نقره می توان فلزات دیگری از قبیل سدیم، آنتیموان و قلع نیز بکار برد تا SO تولید شود.
روش تهیه دیگر برای SO استفاده از اثر بخار گوگرد بر روی SO2 و همچنین انجام عمل تخلیه الکتریکی در گاز SO2 می باشد.
نویسنده: علی نیکخو
ویرایش: کیان کیانی
ادامه دارد…
دیگر مطالب مرتبط با گوگرد
برای سهولت در بازبینی وب سایت شیمی کیمیکال و ده ها وب سایت شیمی ایرانی و خارجی دیگر و شبکه های اجتماعی مرتبط و همچنین سهولت در به اشتراک گذاری مطالب آن ها اپلیکیشن رایگان کیمیکال پلاس را نصب کنید.