دما و یکا های اندازه گیری آن

حقایق شیمی(عناصر)
اسفند ۱, ۱۳۹۵
حقایق شیمی(عناصر)
اسفند ۲, ۱۳۹۵دما یکی از ویژگی های ماده است که میزان گرمی و سردی آن را نشان می دهد و جهت جریان گرما را مشخص می کند. اگر دو جسم دارای دمای متفاوت باشند، انرژی گرمایی از جسم گرم تر به جسم سرد تر منتقل میشود تا هنگامی که دمای دو جسم به تعادل برسد ودرکل هر چقدر اختلاف دما بیشتر باشد انتقال گرما بیشتر است و انتقال تا جایی ادامه دارد که دو جسم به تعادل گرمایی برسند. وبه آن جسمی که دمای بیشتری دارد چشمه ی گرم و به آن جسمی که دمای کمتری دارد چشمه ی سرد میگویند. دما نقش مهمی در همه زمینه های علوم طبیعی شامل فیزیک، زمین شناسی، شیمی، علوم جوی، زیست شناسی و … دارد
بسیاری از خواص مواد شامل جامد، مایع، گاز یا پلاسما، چگالی، حلالیت، فشار بخار و رسانایی الکتریکی به دما بستگی دارد. دما نقش مهمی در انجام و سرعت واکنش های شیمیایی دارد. همچنین میزان حرارت تشعشعی از یک سطح را تعیین می کند. که یک نمونه آن اثر نور لامپ رشته ای است که در آن یک رشته تنگستن الکتریکی دمایش بالا رفته و از خود نور ساطع می کند.
یکاهای گوناگونی برای اندازهگیری دما تعریف شدهاند. در دستگاه بینالمللی از یکای کلوین (k) استفاده میشود؛ ولی یکاهای دیگری مانند سلسیوس (C) و فارنهایت (F) و رانکین (F) نیز برای اندازهگیری دما به کار میروند که در ایران از سلسیوس یا سانتی گراد استفاده میشود.
اندازه گیری دما با استفاده از دماسنج انجام میشود. انواع مختلف دماسنج وجود دارند که از روش های گوناگون برای اندازه گیری دما استفاده می کنند. برای نمونه، اندازه گیری دما در دماسنج جیوه ای با بهره گیری از ویژگی انبساط گرمایی جیوه انجام میشود کمیت دما با وسیله ای به نام دماسنج کالیبره شده اندازه گیری می شود. در اکثر نقاط جهان (به جز بلیز، میانمار، لیبریا و ایالات متحده امریکا) مقیاس سانتی گراد یا سلسیوس برای اندازه گیری دما مورد استفاده قرار می گیرد. بسیاری از دانشمندان جهت اندازه گیری دما در علم ترمودینامیک از کلوین استفاده می کنند. همانطور که می دانیم وقتی که ارتفاع افزایش می یابد (از سطح دریا ) فشار کاهش یافته و با کاهش فشار نقطه جوش آب نیز کاهش خواهد یافت یعنی آب زودتر بجوش می یابد.
تغییر دمای یک جسم یا یک محیط مادی با فرایند تبدیل انرژی انجام میشود. برای نمونه، اتلاف انرژی مکانیکی در اثر اصطکاک منجر به افزایش دما میشود. از سوی دیگر، سرد کردن گازها با انبساط گاز (که انرژی گرمایی به کار تبدیل میشود) انجام می شود.علم ترمودینامیک، به مطالعه فرآیندهای مربوط به تغییرات دما می پردازد.
یکاهای اندازه گیری
یکاهای گوناگونی برای اندازهگیری دما تعریف شدهاند. تفاوت یکاهای مختلف، در دو عامل نقطه صفر یکا و نرخ تغییر واحد یا درجه هر یکا است.
سلسیوس
یکای سلسیوس که به افتخار آندرس سلسیوس نامگذاری شده و با نماد C° نشان داده میشود، متداول ترین یکای مورد استفاده در حال حاضر است. این یکا پیشتر با نام سانتیگراد شناخته می شد که ترکیب دو واژه سانتی (به لاتین: centum) به معنی صد و گراد (به لاتین: gradius) به معنی درجه است. مبنای این یکا، نقطه ذوب و جوش آب هستند. نقطه ذوب آب برابر دمای صفر درجه و نقطه جوش آن برابر دمای صد درجه سانتیگراد تعریف شدهاست.
فارنهایت
فارنهایت با نماد F°، یکای دیگری برای اندازهگیری دما است که در گذشته، در بسیاری از کشورها به کار گرفته می شد و اکنون در کشورهای اندکی از جمله ایالات متحده آمریکا همچنان به عنوان یکای اصلی اندازه گیری دما به کار می رود. نقطه صفری که گابریل دنیل فارنهایت انتخاب کرد عبارت بود از دمای تعادل گرمایی مخلوطی با نسبت برابر از یخ، آب و آمونیوم کلرید (که مقدار آن برابر ۱۷٫۷۸- سلسیوس است). همچنین دو نقطه مرجع دیگر را دمای تعادل گرمایی مخلوط آب و یخ (دمای صفر درجه سلسیوس) به معادل ۳۲ درجه فارنهایت و دمای بدن انسان معادل ۹۸.۶ درجه فارنهایت در نظر گرفت. فارنهایت دریافت که دمای جوش آب با این یکا برابر ۲۱۲ درجه است.
کلوین
یکای اصلی سیستم متریک، کلوین با نماد K است و یکای مطلق دما نامیده میشود زیرا نقطه صفر آن، صفر مطلق است و دمایی پایین تر از آن وجود ندارد کلوین دمای مطلق نامیده می شود و واحد اندازه گیری در SI است به عبارت دیگر، در صفر کلوین هیچ گرمایی وجود ندارد و ذرات ماده از حرکت (که نشان دهنده میزان انرژی گرمایی ذره است) بازمی ایستند به بیان دیگر اتم ها از ارتعاش خود باز می ایستند نرخ تغییرات کلوین، معادل با درجه سلسیوس است و صفر آن برابر ۲۷۳٫۱۵- درجه سلسیوس میباشد و پایین ترین درجه ای است که بشر به آن دست یافته .
رویکرد ترمودینامیکی به دما
دما یکی از مهم ترین کمیت ها در علم ترمودینامیک است. این علم به بررسی ارتباط میان کار و گرما می پردازد. مقیاس خاص در این مورد که دمای مطلق نامیده می شود ارتباط میان دما و کار را بیان می کند. در ترمودینامیک درجه حرارت یک متغیر فشرده ماکروسکوپیک است که دلیل آن مستقل بودن از میزان اتم ها، مولکول ها یا الکترون هاست. در دنیای واقعی اغلب سیستم ها در تعادل ترمودینامیکی و همگن نمی باشند ولی در مطالعات ترمودینامیک کلاسیک برگشت ناپذیر معمولا فضاها را به سلول های کوچک تقسیم می کنند که اگر شرایط تعادل ترمودینامیکی کلاسیک ماده به خوبی تقریب زده شود آن را همگن و درجه حرارت آن را متعادل فرض می کنیم و به آن ترمودینامیکی محلی گویند.
نظر ترمودینامیکی، یکاهای اندازهگیری دما به دو دسته تقسیم می شوند:
مقیاس های تجربی
بسیاری از مقیاس های اندازهگیری دما، به صورت تجربی و بر اساس اندازهگیری ویژگی های فیزیکی مواد، تعریف شدهاند. برای نمونه، ارتفاع ستون جیوه در یک محفظه شیشهای وابسته به دما است و این مطلب، پایه کاربرد دماسنج جیوه ای است. چنین ویژگیهایی دارای محدودیت هستند. برای نمونه، دماسنج جیوه ای نمیتواند دماهای بالاتر از نقطه جوش و پایینتر از نقطه ذوب جیوه را نشان دهد. زیرا در چنین دماهایی گذار فاز جیوه رخ میدهد. همچنین در بعضی از مواد، با افزایش دما به جای افزایش حجم، کاهش حجم انجام میشود.
مقیاسهای نظری
مقیاسهای نظری بر پایه پارامترهای نظری از جمله ترمودینامیک و مکانیک کوانتوم تعریف می شوند. در این مقیاسها از ویژگی مواد و تجهیزات ایدهآل استفاده میشود. برای نمونه، یکای استاندارد دما بر پایه فرایند چرخه ایدهآل ماشین گرمایی کارنو است.
ماده ایدهآلی که میتواند برای تعریف مقیاسهای دما به کار رود، گاز کامل است. فشار یک توده گاز کامل با حجم و جرم ثابت، نسبت مستقیمی با دمای آن دارد. برخی از گازهای طبیعی در دمای معمول، ویژگیهایی نزدیک به گاز کامل دارند.
اندازه گیری طیف تابش الکترومغناطیسی از یک جسم سیاه سه بعدی ایدهآل میتواند مقدار دقیق دما را به دست دهد، زیرا بسامد پیشینه طیف تابیده از یک جسم سیاه، نسبت مستقیم با دمای جسم سیاه دارد.
برخی از دماهای مهم
دما بر حسب درجه سلسیوس
۱ نقطه ی جوش هیدروژن مایع ۲۳۵-
۲ نقطه ی انجماد الکل ۱۱۶-
۳ نقطه ی انجماد جیوه ۳۹-
۴ نقطه ی جوش اکسیژن مایع ۳۲-
۵ نقطه ی ذوب یخ ۰
۶ دمای بدن انسان سالم ۳۷
۷ نقطه ی جوش الکل ۷۹
۸ نقطه ی جوش آب ۱۰۰
۹ نقطه ی جوش جیوه ۳۵۷
۱۰ نقطه ی ذوب طلا ۱۰۶۷
۱۱ دمای هسته ی زمین ۳۷۰۰
۱۲ دمای سطح خورشید ۵۷۰۰
نقطه سه گانه آب 273.16 کلوین است و این نقطه دمای استاندارد بین المللی نامیده می شود. نقطه انجماد آب در فشار اتمسفر، 0 درجه سلسیوس است که 0.01 کلوین کمتر از 273.15 می باشد. اما اگر می خواهید در این مورد واقعا دقیق باشید نقطه جوش آب 373.125 کلوین یا 99.975 درجه سلسیوس است
ظرفیت گرمایی
هنگامی که به یک نمونه حرارت داده می شود به این معنی است که جسم از یک منبع خارجی انرژی حرارتی دریافت می کنند برخی از این حرارت داده شده به انرژی جنبشی در جسم تبدیل شده و بقیه فرم های انرژی به یک خاصیت در مواد تبدیل می شود. انرژی جنبشی باعث افزایش دمای جسم می گردد. به مقدار حرارت تولید شده ( ΔQ )تقسیم بر تغییر دمای جسم ΔT)) (سلسیوس)، ظرفیت گرمایی آن ماده می گویند. به زبانی ساده تر آن که یک جسم بر اثر حرارت چه میزان تغییر دما می تواند داشته باشد.
C=ΔQ / ΔT.
دمای جوش آب
فارنهایت سلسیوس کلوین
212ºF 100ºC 373.15K
دمای انجماد آب
فارنهایت سلسیوس کلوین
32ºF 0ºC 273.15K
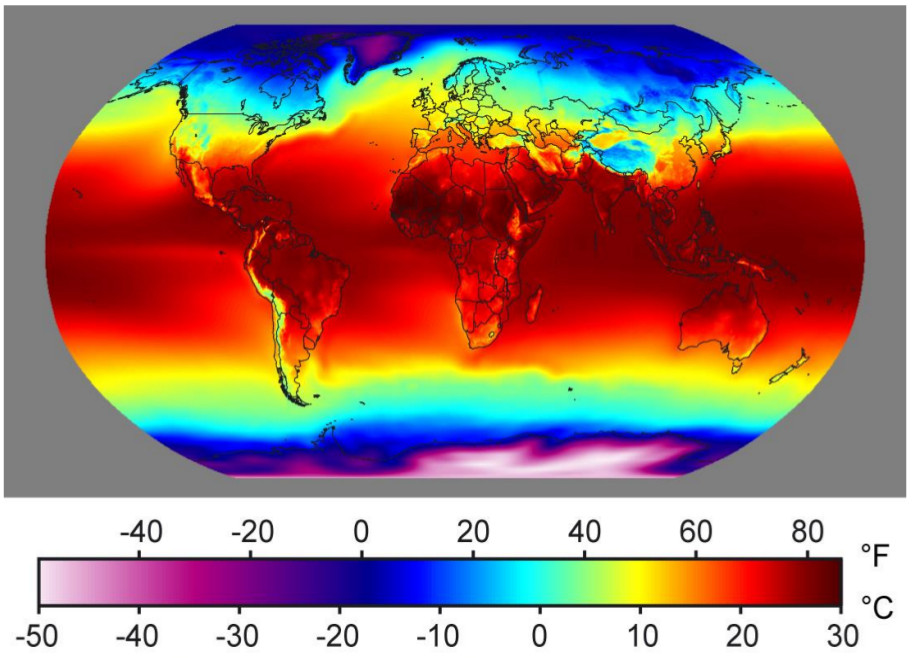
متوسط درجه حرارت سالانه در سراسر جهان
دما سنج
نخستین وسیله واقعی علمی را برای اندازهگیری درجه حرارت در سال ۱۵۹۲ گالیله اختراع کرد وی برای این منظور یک بطری شیشهای گردن باریک انتخاب کرده بود. بطری با آب رنگین تا نیمه پر شده و وارونه در یک ظرف محتوی آب رنگ قرار گرفته بود. با تغییر دما هوای محتوی بطری منبسط یا منقبض می شد و ستون آب در گردن بطری بالا یا پایین می رفت. وسیله گالیله مقیاسی واقعی برای سنجش دما نبود به طوری که وسیله وی بیشتر جنبه دما نما داشت. تا جنبه دماسنج در سال ۱۶۳۱ری تغییراتی را در دمانگار گالیله پیشنهاد کرد. پیشنهاد وی همان بطری وارونه گالیله بود که در آن فقط سرد و گرم شدن از روی انقباض و انبساط آب ثبت می شد.
در سال ۱۶۳۵ دوک فردینالند توسکانی، که به علوم علاقه مند بود دما سنجی ساخت که در آن از الکل (که در دمایی خیلی پایینتر از دمای آب یخ میبندد.) استفاده کرد. و سر لوله را چنان محکم بست که الکل نتواند تبخیر شود. سرانجام در سال ۱۶۴۰ دانشمندان آکادمی لینچی در ایتالیا نمونهای از دماسنج های جدیدی را ساختند که در آن جیوه به کار برده و هوا را دست کم تا حدودی از قسمت بالای لوله بسته خارج کرده بودند. توجه به این نکته جالب است که در حدود نیم قرن طول کشید تا دماسنج کاملاً تکامل یافت.
محدوده کاری دما سنج
باید توجه داشت که با ترمومترهای جیوه ای نمی توان سرما های کمتر از ۳۵ درجه زیر صفر را اندازه گیری کرد زیرا جیوه در ۳۹ – درجه سانتی گراد منجمد میشود. از این روی برای اندازه گیری سرما های شدید از ترمومترهای الکلی استفاده می کنند زیرا الکل در منفی ۱۲۰ درجه سانتی گراد مایع است و بالعکس در ۷۸ درجه سانتی گراد بجوش می آید از این روی ترمومتر ماگزیما و مینیما را بطور مرکب بکار می برند که از الکل و جیوه تشکیل می یابد این نوع میزان الحراره می تواند حداکثر درجه حرارت و حداقل آنرا در مدت معینی مثلا یک شبانه روز تعیین کند و از یک میزان الحراره الکلی دراز تشکیل شده است و برای اینکه جای زیاد نگیرد ساقه آنرا دو مرتبه خم کرده اند و در قسمت خمیده آن که بشکل «ایو»ی فرانسه می باشد جیوه ریخته شده و بدین ترتیب الکل به دو قسمت تقسیم می شود: یک قسمت در طرف راست لوله باقی می ماند که بالای آن حباب خالی از هواست کمی الکل در آن بخار می شود و طرف چپ آن منتهی به مخزن الکل است . در بالای دو طرف جیوه دوسوزن فولادی موسوم به نشانه قرار دارد.
منابع:
1-کتاب عملیات دستگاه ها در صنایع شیمیایی (فصل دوم)
2-http://www.wikipedia.com
3- www.allmeasures.com/temperature.html
پژوهش گر: ایمان انصاری







4 Comments
سلام.وبسایت خیلی خوبی دارید.دستتون درد نکنه
سلام.مطالب خوبی دارین-مطالب مربوط به یک موضوع مثلا عواما فیزیکی یا شیمیایی و… محیط کار مجزا شوند خیلی بهتر میشود.وسپاسگزارم-مهندس تیموری-مدرسHSE
بسیار مفید بود، خیلی از مطالب استفاده کردم. ممنون
خیلی کامل بود