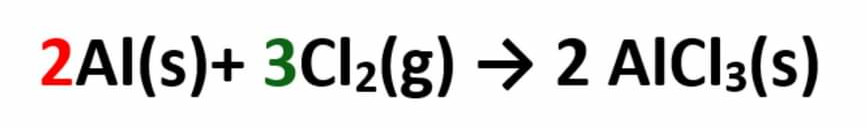سه روش برای پیدا کردن واکنش دهنده محدود کننده، محصول تئوری
دوره اختر شیمی
دی ۲۳, ۱۴۰۱
خورشید و گداخت هسته ای
فروردین ۲۱, ۱۴۰۲سه روش برای پیدا کردن واکنش دهنده محدود کننده، محصول تئوری
پیدا کنید واکنش دهنده محدود کننده را وقتی که ۲/۸ گرم نمونه آلومینیم با ۴/۱۵ گرم کلر مطابق معادله زیر واکنش می دهد:
واکنش دهنده محدود کننده به نسبت مولی بستگی دارد نه به جرم واکنش دهنده
روش ۱- مقایسه نسبت استاندارد و نسبت واقعی
نسبت واقعی(۱/۷۸) بزرگتر از نسبت استاندارد (۰/۶۶۷) است که نشان دهنده این است که مول های آلومینیم بیشتر و مول های کلر کمتر از مقدار لازم است. پس کلر محدود کننده است.
روش ۲- پیدا کنید چقدر یک واکنش دهنده لازم است تا واکنش دهنده دیگر به طور کامل مصرف شود.
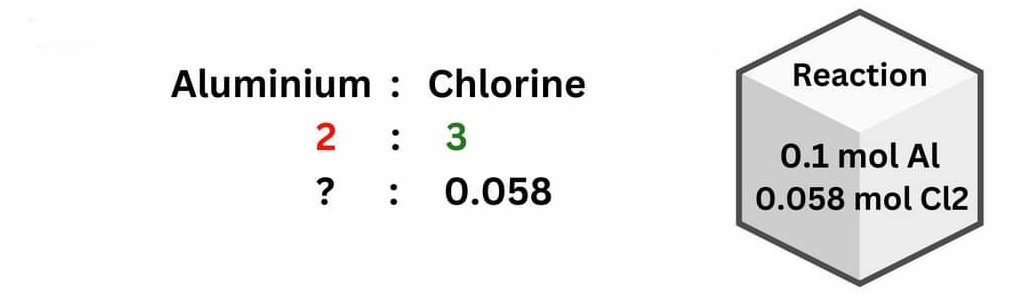
مقدار ۰/۱۵ مول کلر لازم است تا همه ی ۰/۱ مول آلومینیوم مصرف شود اما مقدار واقعی ۰/۰۵۸ مول کمتر از مقدار لازم است پس کلر محدود کننده است.
همین محاسبه می تواند برای آلومینیم به جای کلر انجام شود.
مقدار ۰/۰۳۸۷ از آلومینیم لازم است تا ۰/۰۵۸ مول کلر کامل مصرف شود اما مقدار واقعی آلومینیم ۰/۱ مول است که از مقدار لازم بیشتر است پس آلومینیم محدود کننده نیست.
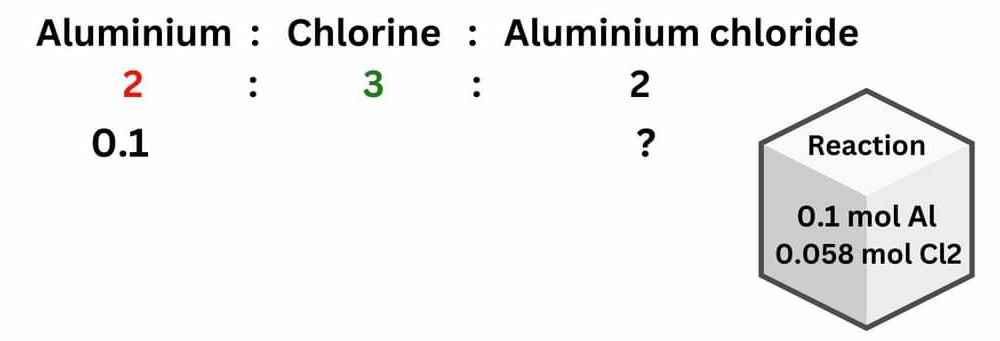
روش ۳- واکنش دهنده ای را پیدا کنید که مقدار کمتری فراورده می دهد.
مقدار فراورده ۰/۱ مول
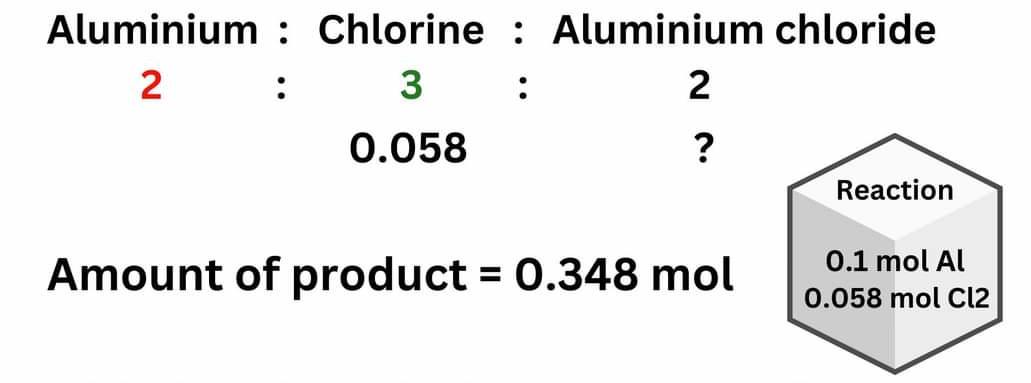
مقدار فراورده ۰/۳۴۸ مول
پس کلر مقدار کمتری فراورده می دهد پس کلر محدود کننده است
مقدار ۰/۳۴۸ مول از فراورده که واکنش دهنده محدود کننده کامل مصرف می شود.
نویسنده:
Nahid Alshennawy