تفاوت باز با قلیا

پاورپوینت شیمی رنگ
دی ۲۳, ۱۳۹۶
معرفی نرم افزارهای رایگان به جای ویزیو visio
بهمن ۱۵, ۱۳۹۶قلیایی ها همانند باز ها اسیدها را خنثی می کنند اما قلیایی ها در آب یون هیدرواکسید منفی(OH–) تولید می کنند، در حالیکه باز ها مثل مس اکسید یا آهن اکسید در آب OH– تولید نمی کنند و همچنین در آب حل نمی شوند.
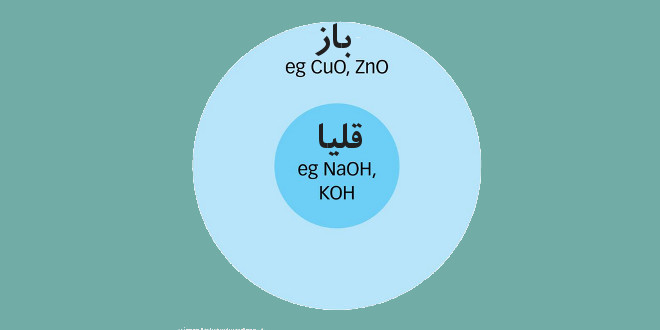
همه ی قلیایی ها باز هستند اما همه ی بازها قلیایی نیستند.
چند مثال برای قلیا:
۱- محلول سدیم هیدرواکسید NaOH
۲- محلول کلسیم هیدرواکسید Ca(OH)2
۳- محلول آمونیاک NH3
و اما درباره ی بازها:
گفتیم ماده ای است که اسید را خنثی می کند اما یون هیدرواکسید منفی تولید نمی کند و در آب حل نمی شوند
چند مثال برای بازها: مس اکسید، آهن اکسید و روی کربنات
ویژگی قلیایی ها: در آب محلول هستند و OH– تولید می کنند.
ویژگی بازها: در آب محلول نیستند و OH– تولید نمی کنند.
شباهت قلیایی ها و بازها: هر دو اسید ها را خنثی می کنند.
دانلود اپلیکیشن اندرویدی محلول ها از مارکت کیان دروید و بازار:
سرچشمه:
https://socratic.org/questions/how-to-differentiate-between-bases-and-alkali




3 Comments
چطورحل نمیشه؟اکسیدهای فلزی موقعی ک وارد اب میشن ب یونی نلدیل و سپس ب یونهای خود تفکیک میشن
سلام
خب تمام اکسیدهای فلزی این خاصیت رو ندارن
مثلا MgoH اکسید فلزی ای است که در آب حل نشده و رسوب میکنه
دم شما گرم