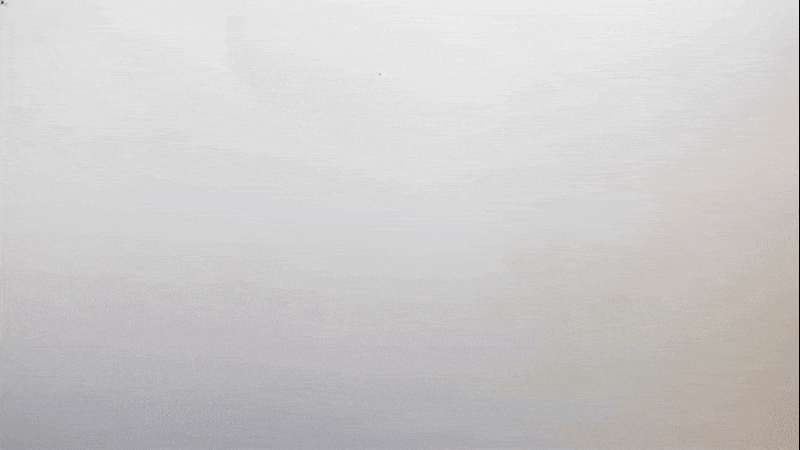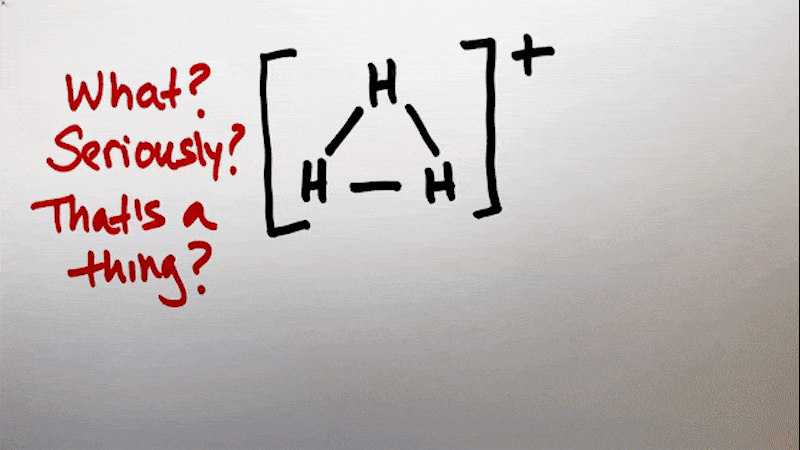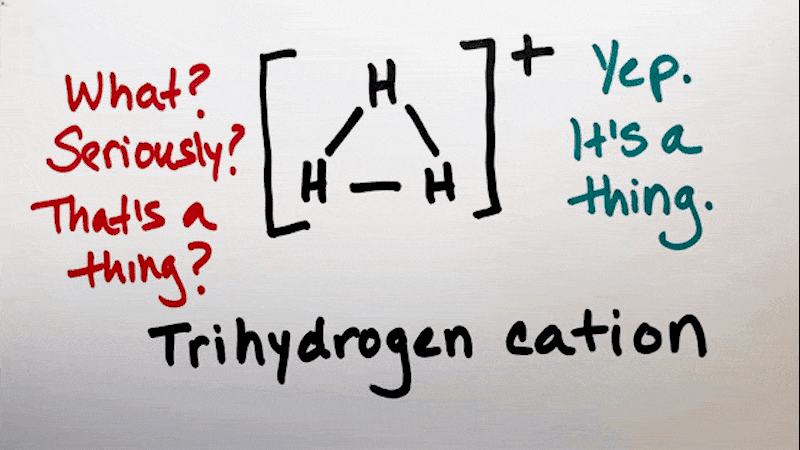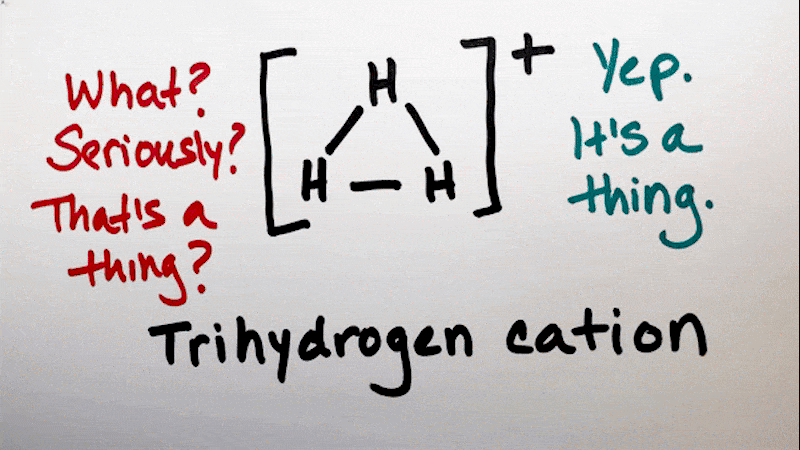فولرن ها در طبیعت و در فضا
اسفند 12, 1403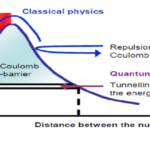
سد کولن
فروردین 7, 1404کاتیون تری هیدروژن، H3+، یک یون مولکولی پایه است که در بسیاری از محیط های اخترفیزیکی یافت می شود. نقش مهمی در شیمی بین ستاره ای و تشکیل مولکول های پیچیده تر ایفا می کند. در اینجا نگاهی دقیق به H3+ در فضا داریم:
کاتیون H3+ چیست؟
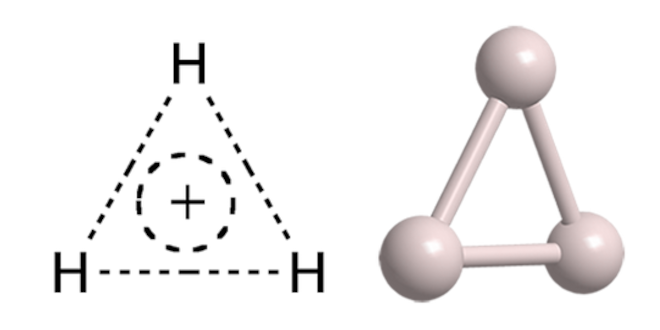
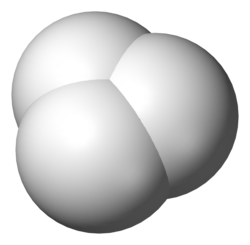
• ترکیب: H3+ از سه پروتون (هسته هیدروژن) و دو الکترون تشکیل شده است.
• ساختار: دارای ساختار مثلثی متساوی الاضلاع است.
• کشف: اولین بار در آزمایشگاه در سال 1911 توسط جی جی تامسون
فیزیکدان بریتانیایی، جی. جی. تامسون، برای اولین بار در سال ۱۹۱۱، H3+ را در یک لوله پلاسما در آزمایشگاه خود با استفاده از نوعی اولیه از طیفسنجی جرمی کشف کرد . تا دهه ۱۹۶۰، دانشمندان حدس میزدند که H3+ ممکن است در فضا یافت شود، اما در سال ۱۹۸۹ بود که محققان سیگنال مشخصه آن را که از مشتری میآمد، مشاهده کردند.
او هنگام استفاده از نوعی اولیه از طیفسنجی جرمی برای مطالعه گونههای حاصل از تخلیههای پلاسما ، مقدار زیادی یون چند اتمی با نسبت جرم به بار ۳ را کشف کرد. او اظهار داشت که تنها دو احتمال وجود دارد: C4+ یا H3+ از آنجایی که سیگنال در گاز هیدروژن خالص قویتر میشد ، او به درستی گونه را H3+ تعیین کرد..
یک دستگاه اسپکتروسکوپ جرمی اولیه:
اهمیت کاتیون تری هیدروژن در محیط های اخترفیزیکی:
کاتیون H3+ به چند دلیل یکی از مهم ترین یون های مولکولی در جهان در نظر گرفته می شود:
1. فراوانی: در مناطقی که هیدروژن مولکولی (H2) وجود دارد و توسط پرتوهای کیهانی یا اشعه ماوراء بنفش یونیزه می شود، نسبتاً فراوان است.
2. عامل پروتوناسیون(پروتون دار کردن): این یک پروتوناتور(پرتون دار کننده) بسیار کارآمد است، به این معنی که به راحتی یک پروتون (H+) را به مولکول های دیگر منتقل می کند. این فرآیند واکنش های شیمیایی زیادی را آغاز می کند که منجر به تشکیل مولکول های پیچیده تر می شود.
3. مخزن انرژی: انرژی حاصل از پرتوهای یونیزان را به طور موثر به انرژی شیمیایی تبدیل می کند.
چی؟ جدی میگی؟ یه همچین چیزی واقعآ وجود داره؟
بله وجود داره.
اسمش: کاتیون تری هیدروژن هست.
مسیرهای تشکیل کاتیون تری هیدروژن:
کاتیون H3+ در مرحله اول از طریق واکنش های زیر تشکیل می شود:
1. یونیزاسیون H2: پرتوهای کیهانی یا فوتون های UV هیدروژن مولکولی (H2) را یونیزه می کنند:
H₂ + cosmic ray/UV photon → H₂⁺ + e⁻
2. واکنش کاتیون دی هیدروژن با H2: یون H2+ بهسرعت با مولکول H2 دیگر واکنش میدهد:
H₂⁺ + H₂ → H₃⁺ + H
مسیرهای تخریب:
کاتیون H3+ در درجه اول از طریق واکنش با مولکول های دیگر، به ویژه گونه های فراوان مانند مونوکسید کربن (CO) و آب (H2O) از بین می رود:
• واکنش با CO:
H₃⁺ + CO → HCO⁺ + H₂
* واکنش با H2O:
H₃⁺ + H₂O → H₃O⁺ + H₂
یونهای HCO+ و H3O+میتوانند در واکنش های بعدی شرکت کنند تا مولکولهای پیچیدهتری تشکیل دهند.
• نوترکیبی تجزیه ای:H3+ همچنین می تواند با واکنش با الکترون ها از بین برود (نوترکیبی تجزیه ای)، اگرچه این فرآیند به طور کلی کارایی کمتری نسبت به واکنش با سایر مولکول ها دارد:
H₃⁺ + e⁻ → H + H + H or H₂ + H
روش های تشخیص کاتیون تری هیدروژن:
کاتیون H3+ در فضا از طریق طیفسنجی فروسرخ (IR) شناسایی میشود. این انتقال ارتعاشی چرخشی مشخص در مناطق مادون قرمز نزدیک و مادون قرمز میانی دارد.
• تلسکوپهای فروسرخ: تلسکوپهایی مانند تلسکوپ بسیار بزرگ (VLT)، رصدخانه کک، و تأسیسات تلسکوپ فروسرخ (IRTF) برای تشخیص H3+ استفاده شدهاند.
• چالش های مشاهده کاتیون تری هیدروژن: تشخیص H3+ به دلیل خطوط جذب نسبتا ضعیف و وجود گونه های جاذب دیگر در جو می تواند چالش برانگیز باشد. مشاهدات اغلب از سایت های در ارتفاع بالا یا تلسکوپ های فضایی انجام می شود.
محیط هایی که در آن H3+ یافت می شود:
کاتیون H3+ در انواع محیط های اخترفیزیکی شناسایی شده است از جمله:
• ابرهای پراکنده بین ستاره ای: این ابرهای گاز و غبار کم چگالی هستند که توسط ستاره های پس زمینه روشن می شوند.
• ابرهای مولکولی متراکم: این مناطق سرد و متراکم هستند که در آن ستاره ها متولد می شوند.
• دیسک های پیش سیاره ای: این ها قرص های چرخان از گاز و غبار در اطراف ستاره های جوان هستند که در آن سیارات در حال شکل گیری هستند.
• مراکز کهکشانی: H3+ در نواحی مرکزی کهکشان ها، از جمله راه شیری خودمان، شناسایی شده است.
• بقایای ابرنواختر: این پوسته های گاز در حال انبساط هستند که توسط ستاره های در حال انفجار به بیرون پرتاب می شوند.
• جو سیارات فراخورشیدی: پتانسیل برای تشخیص H3+ در جو سیارات فراخورشیدی وجود دارد.
نقش کاتیون تری هیدروژن در واکنش های شیمیایی در فضا:
کاتیون H3+ واکنش های شیمیایی زیادی را آغاز می کند که منجر به تشکیل مولکول های پیچیده تر می شود، از جمله:
• تشکیل HCO+: همانطور که در بالا ذکر شد ، H3+ با CO واکنش می دهد تا HCO+، یک پیش ساز کلیدی برای سایر مولکول های حاوی کربن تشکیل شود.
• تشکیل H2O+ و H3O+: واکنش با H2O منجر بهH2O+ و به دنبال آن H3O+ می شود که برای شیمی اکسیژن بسیار مهم است.
• تشکیل مولکول های آلی: واکنش های H3+ با مولکول های دیگر می تواند منجر به تشکیل مولکول هایی نظیر، متانول (CH3OH)، فرمالدئید (H2CO) و سایر ترکیبات آلی شود.
پیامدهای اخترشیمی:
• درک فراوانی مولکولی: با مطالعه فراوانی H3+ و واکنش های آن، اخترشناسان می توانند بینشی در مورد فرآیندهای شیمیایی که بر تشکیل مولکول ها در محیط های مختلف اخترفیزیکی حاکم است، به دست آورند.
• بررسی شرایط فیزیکی: فراوانی H3+ به شرایط فیزیکی (چگالی، دما، سرعت یونیزاسیون) گاز حساس است. می توان از آن به عنوان کاوشگر این شرایط استفاده کرد.
• ردیابی یونیزاسیون پرتوهای کیهانی: از آنجایی که پرتوهای کیهانی منبع اولیه تشکیل H3+ هستند، فراوانی آن می تواند برای ردیابی نفوذ پرتوهای کیهانی به ابرهای مولکولی استفاده شود.
کشف H3+ در فضا به توصیف طیف این مولکول وابسته بود، که بخشهایی از آن در سال ۱۹۸۰ توسط تاکشی اوکا از دانشگاه شیکاگو تعریف شده بود. این مولکول، نور مادون قرمز را در طول موجهای مشخصی تابش میکند که میتوانند در فواصل وسیع فضا نفوذ کنند و بدون هیچ مانعی به آشکارسازهای روی زمین برسند. نکته مهم این است که این یون، قویترین تابشهای خود را در مجموعهای از طول موجها منتشر میکند که به ندرت توسط سایر مولکولها تابش میشود، و این امر، تشخیص آن را حتی در فاصله سالهای نوری، نسبتاً آسان میکند.
عکسی فروسرخ از منطقهی ستارهزایی صورت فلکی مارافسای.
شکل خاصی از H3+ به دانشمندان این امکان را داد تا سن یکی از این ابرها را در منطقهی ستارهزایی صورت فلکی مارافسای (Ophiuchus) که در اینجا در یک عکس مادون قرمز نشان داده شده است، تخمین بزنند .
تحقیقات آینده:
• مشاهدات با حساسیت بالاتر: تلسکوپ ها و ابزارهای آینده با حساسیت افزایش یافته امکان تشخیص H3+ را در محیط های دورتر و کم نورتر می دهند.
• مطالعات آزمایشگاهی: ادامه مطالعات آزمایشگاهی در مورد واکنش های H3+ با سایر مولکول ها برای بهبود دقت مدل های شیمیایی مورد نیاز است.
• مدل سازی نظری: توسعه مدل های نظری پیچیده تر از شیمی بین ستاره ای به درک بهتر نقش H کمک می کند.
• کاتیون H3+ در تشکیل مولکول های پیچیده.
به طور خلاصه، کاتیون تری هیدروژن (H3+) یک یون مولکولی بنیادی است که نقش مرکزی را در شیمی بسیاری از محیطهای اخترشیمی ایفا میکند. فراوانی، واکنشها و تشخیص آن، دیدگاه های ارزشمندی را در مورد فرآیندهایی که منجر به تشکیل مولکولها در فضا میشوند، ارائه میکند.
سرچشمه:
https://www.acs.org
https://en.wikipedia.org
https://cen.acs.org