ویژگی های مشترک عناصر واسطه

تولید رنگ فلئورسنت
تیر ۲۶, ۱۳۹۴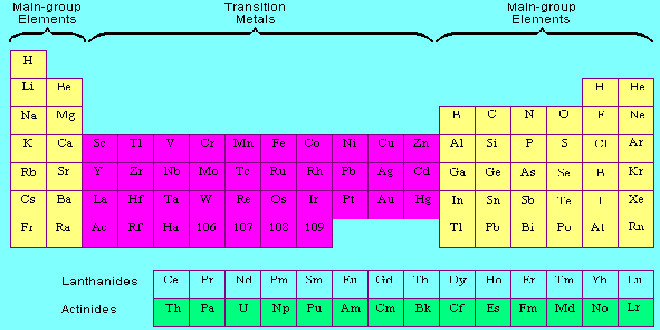
تعیین دوره و گروه عناصر واسطه
تیر ۳۰, ۱۳۹۴۱- اغلب تراز s لایه ظرفیت آنها دو الکترون دارند( به جز کروم، مس، نقره، طلا، ….)
۲- به طور کلی خواص فلزی دارند حرارت و الکتریسیته را به خوبی از خود عبور می دهند و در حرارت معمولی به جز جیوه همه جامد هستند.
۳- بسیاری از آن ها اعداد اکسایش متنوع دارند، مانند منگنز که اعداد اکسایش ۳،۲، ۴، ۶، ۷ دارد(اگرچه همه ی حالت های اکسایش از ۳- تا ۷+ در منگنز مشاهده شده است). زیرا عناصر واسطه علاوه بر الکترون های تراز s تمام یا تعدادی از الکترون های تراز d را نیز در ترکیب شرکت می دهد حد اکثر ظرفیت آن ها از مجموع تعداد الکترون های s و d تجاوز نمی کند.
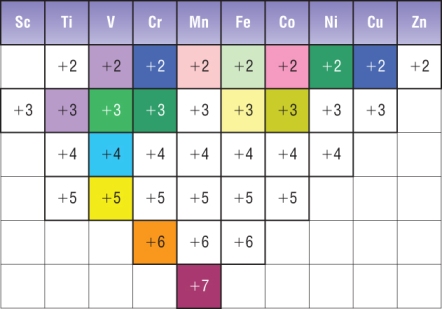
۴- نقطه ذوب و جوش آن ها بالا است زیرا در پیوند فلزی این عناصر علاوه بر الکترون های s ، الکترون های تراز d نیز شرکت می کنند و به علت وابستگی بیشتر به هسته تا حدی پیوند کووالانسی به وجود می آید که باعث استحکام پیوند فلزی می گردد.
۵- تغییرات تدریجی خواص در عناصر واسطه هر دوره نسبت به دوره ی اصلی کمتر است زیرا با افزایش پروتون، الکترون ها به تراز ماقبل آخر افزوده می شود در نتیجه نیروی دافعه ی این تراز بر تراز آخر زیاد شده و از تغییر شدید خواص جلوگیری می کند. مثلآ تغییر شعاع در هر ردیف واسطه از ردیف اصلی بسیار کمتر است.
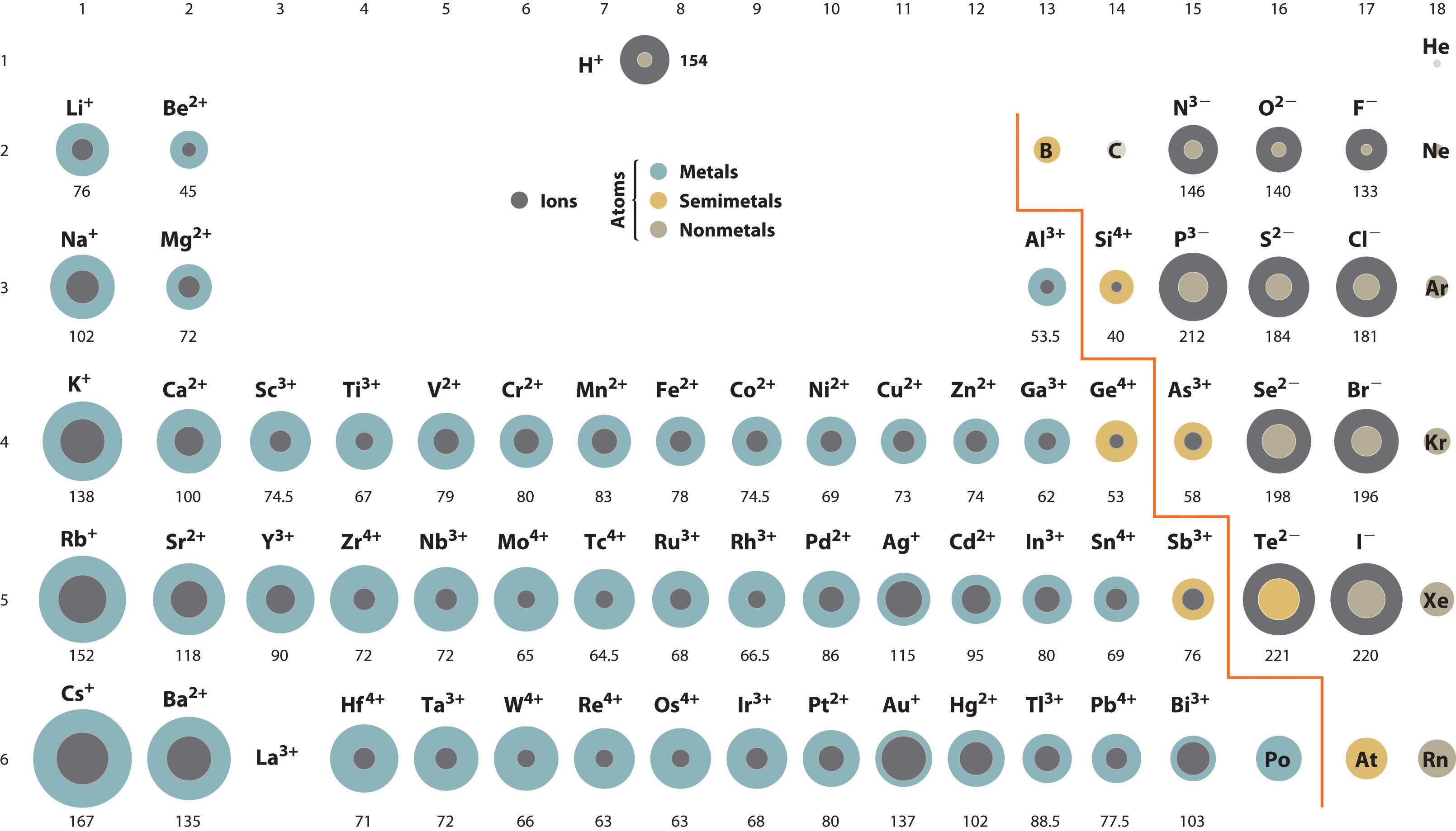
۶- عمدتآ ترکیبات رنگین دارند.
۷- در تشکیل ترکیبات کمپلکس شرکت می کنند. به این ترتیب که یون عنصر واسطه توسط تعدادی از یون ها یا مولکول های قطبی دیگر احاطه شده ترکیبات پیچیده تشکیل می دهند که کمپلکس نام دارد.
۸- عمومآ پارا مغناطیس هستند زیرا در اغلب حالت های اکسایش خود الکنرون های جفت نشده دارند.
۹- اغلب به عنوان کاتالیزگر استفاده می شوند.
۱۰- در عناصر واسطه به طور کلی با افزایش تعداد اربیتال های نیمه پر در لایه ظرفیت دمای ذوب افزایش می یابد.
دانلود برنامه های ما در مارکت کیان دروید
سرچشمه ها:
www.chemhume.co.uk
images.fineartamerica.com
https://en.wikipedia.org
http://www.compoundchem.com/