نکات کنکوری شیمی ۲۳(واکنش منگنز دی اکسید و هیدروکلریک اسید)

نکات کنکوری شیمی ۲۲(واکنش پرمنگنات با گوگرد دی اکسید)
فروردین ۱۸, ۱۳۹۷
سود پرک
فروردین ۲۰, ۱۳۹۷یک گرم منگنز دی اکسید نا خالص با هیدروکلریک اسید ۲۵۰ سانتی متر مکعب گاز کلر می دهد در صورتی که حجم مولی گاز کلر در شرایط آزمایش ۲۵ لیتر باشد درصد خلوص این نمونه منگنز دی اکسید کدام است؟(سراسری تجربی سال ۶۵)
Cl=35.5 , O=16 , Mn=55 , H=1
۱) ۴۳/۵
۲) ۵۵
۳) ۷۱
۴) ۸۷
برای حل این تست ابتدا باید معادله موازنه شده واکنش هیدروکلریک اسید را با منگز دی اکسید بنویسیم ولی پیش از آن باید یک نکته را درباره این مسئله متذکر شویم
همانطور که می دانید حجم مولی گازها در شرایط استاندارد( صفر درجه سانتیگراد و فشار یک اتمسفر) برابر ۲۲/۴ لیتر می باشد که این عدد را ما باید به خاطر بسپاریم.
اما اگر شرایط استاندارد نباشد در صورت مسئله باید به آن اشاره کنند مثل همین مسئله که حجم مولی را ۲۵ لیتر گفته است. یعنی یک مول از گاز در شرایط آزمایش ۲۵ لیتر حجم اشغال می کند.
خوب اکنون معادله موازنه شده این واکنش را می نویسیم:
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
نوشتن و موازنه ی واکنش های اکسایش کاهش را در اپلیکیشن اکسایش کاهش آموزش داده ایم:

اکنون به دو روش می توانیم جواب را به دست آوریم: روش تناسب که برای کنکور مناسب تر است زیرا ساده تر و سریع تر است و روش استوکیومتری که امروزه در کتاب های درسی متداول شده است.
چون مقدار منگنز دی اکسید را بر حسب گرم داده، ابتدا باید جرم مولکولی MnO2 را به دست آوریم
MnO2=55+2(16)=87
تذکر: میلی لیتر با سانتی متر مکعب و سی سی هر سه با هم برابر اند
روش تناسب:
برای فراگیری محاسبات استوکیومتری اپلیکیشن از اتم تا استوکیومتری را از مارکت کیان دروید یا بازار دانلود و مطالعه کنید:


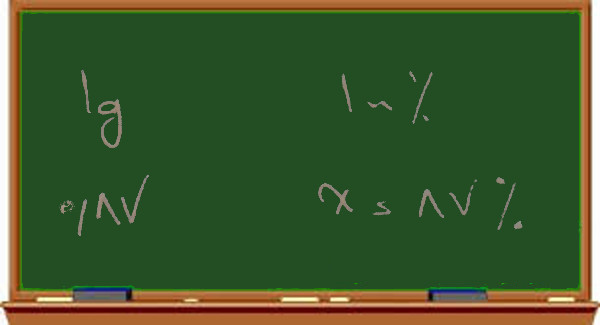
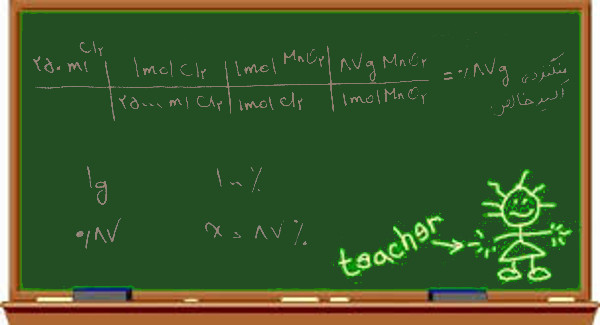



1 Comment
عالی هستید????