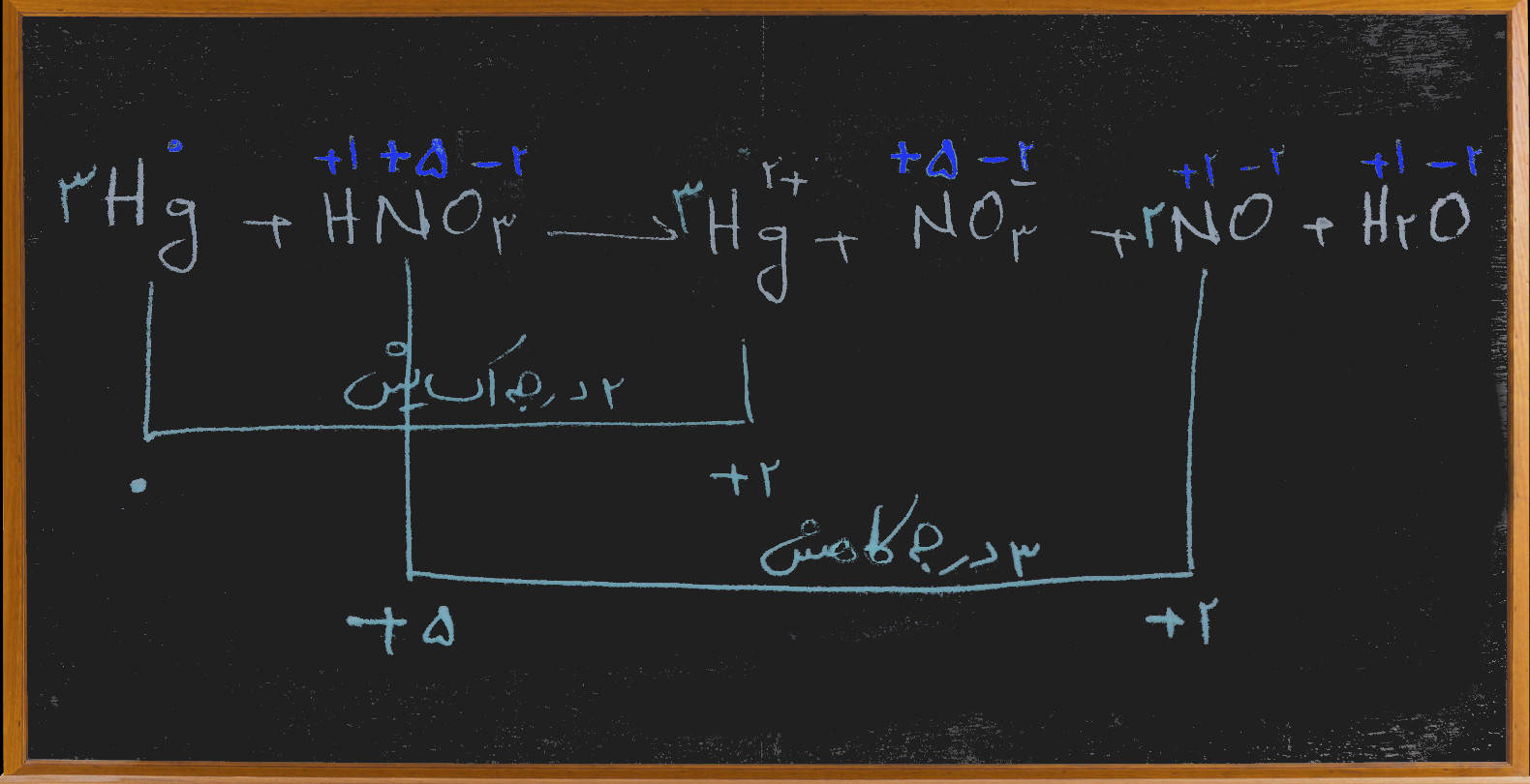نکات کنکوری شیمی ۱۷ (اکسایش کاهش)

رسیدن به پی اچ مورد نظر
مهر ۲۷, ۱۳۹۶
چگونه غلظت سولفوریک اسید را بفهمیم؟
مهر ۲۹, ۱۳۹۶- kian kiani
- kiandroid.ir
- kimical.ir
- آمادگی کنکور شیمی
- آموزش شیمی
- اپلیکیشن اکسایش کاهش
- اپلیکیشن شیمی
- اپلیکیشن های شیمی
- تست شیمی
- تست های شیمی
- تقویتی شیمی
- تمرین های اضافی شیمی
- حا مسائل شیمی یازدهم
- حل تمرین های شیمی دهم
- حل تمرین های شیمی یازدهم
- حل مسائل شیمی دهم
- درس شیمی
- سایت شیمی
- سوالات کنکور شیمی
- شیمی
- شیمی دانشگاهی
- صنایع شیمی
- صنایع شیمیایی
- صنعت شیمی
- کنکور شیمی
- کیان دروید
- کیمیکال
- موازنه اکسایش کاهش
- نکات کنکوری شیمی
- نکته های کنکوری شیمی
- نمونه تمرین های شیمی
- نمونه مسائل شیمی شیمی پیش دانشگاهی
- وب سایت شیمی
ضرایب NO و آب در معادله ی زیر بعد از موازنه به ترتیب عبارت است از:
Hg + HNO3 → Hg2+ + NO3– + NO + H2O
۱) ۳ و ۲
۲) ۲ و ۳
۳) ۲ و ۴
۴) ۶ و ۴
خوب ابتدا باید درجه اکسایش ها را پیدا کنیم سپس عناصری که تغییر درجه داشته اند را باید تغییر درجه آن ها را عوض کنیم یعنی تغییر درجه عنصری که اکسید شده را بدهیم به عنصری که کاهش یافته و بر عکس فقط یکی از نکاتی که این واکنش دارد این است که نیتروژن یک جا تغییر عدد اکسایش داشته NO و جای دیگر نداشتهNO3–
در این مورد ابتدا باید تغییر عدد اکسایش را طرف دوم اعمال کنیم سپس تعداد نیتروژن هایی که تغییر کرده و تغییر نکرده را طرف دوم بشماریم و در طرف اول ضریب مناسب را بنویسیم:
خوب در طرف دوم ضریب Hg مشخص شد که ۳ است که ضریب ۳ را به Hg در طرف اول هم می دهیم و ضریب NO برابر ۲ است اما وپیش از این که ضریب نیتروژن ها در طرف اول را بنویسیم باید ضریب NO3– در طرف اول مشخص شود، اما چگونه؟
این را به خاطر داشته باشید که یک واکنش اکسایش کاهش نه تنها از نظر عنصر و یون بلکه از نظر بار نیز باید موازنه باشد، همان طور که می بینید طرف اول هیچ باری وجود ندارد پس طرف دوم هم جمع جبری بارها باید صفر شود آز آنجایی که ضریب Hg2+ برابر ۳ شده است پس بار مثبت برابر ۳x۲=۶ می شود پس ضریب NO3– هم باید ۶ باشد تا جمع جبری بارهای مثبت و منفی برابر صفر شود. اکنون که ضریب یون نیترات هم مشخص شد همه ی نیتروژن ها را در طرف دوم می شماریم ۶+۲=۸ و به طرف اول اعمال می کنیم و از آنجا با توجه به مشخص شدن تعداد هیدروژن در طرف اول(۸) ضریب ۴ برای آب در طرف دوم می نویسیم تا تعداد هیدروژن در طرف دوم هم ۴x۲=۸ شود.
پس ضریب NO و آب به ترتیب ۲ و چهار (گزینه ی۳) می شود دقت کنید سوال را به گونه ای داده است که شما برای جواب دادن باید تا آخر معادله را موازنه کنید چون ضریب آب آخرین ضریبی است که پیدا می شود.
اپلیکیشن اکسایش کاهش