انفجار سولفوریک اسید و پرمنگنات
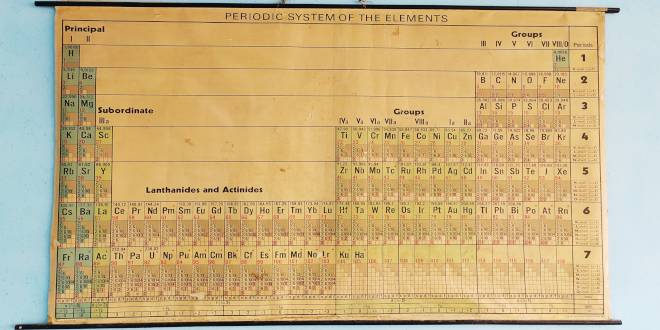
نام های قدیمی ترکیبات شیمیایی
فروردین ۲۸, ۱۳۹۴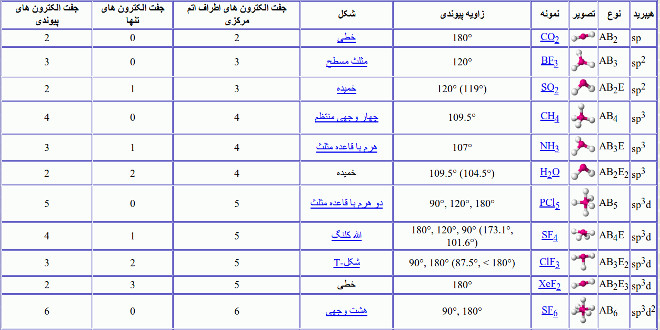
جدول آرایش الکترون نقطه ای
فروردین ۳۰, ۱۳۹۴در آزمایشگاه شیمی همیشه به دانش آموزان تاکید می کنیم اگر می خواهید با یک پیپت از دو محلول بردارید هر بار پیپت را ابتدا با آب شیر بشویید و سپس با آب مقطر آب بکشید و پس از آن محلول را با پیپت بکشید. اما گاهی آن ها این نکته را جدی نمی گیرند.
چند سال پیش شیشه ی سولفورک اسید غلیظ ناگهان وسط آزمایشگاه ترکید و اسید ۹۸٪ بر روی زمین ریخت یکی از دانش آموزان هم پا بر روی این اسید روغنی گذاشت و لیز خورد بر روی زمین خدا رو شکر برای هیچ کس حادثه ای پیش نیامد اما وقتی علت را جستجو کردیم کاشف به عمل آمد یکی از دانش آموزان ابتدا با پیپت پرمنگنات کشیده بود و بدون آن که پیپت را بشوید سولفوریک اسید با همان پیپت برداشته بود و در سولفوریک اسید را بسته بود.
واکنش پرمنگنات با سولفوریک اسید به صورت زیر است:
4KMnO4 + 6H2SO4 → 6H2O + 2K2SO4 + 4MnSO4 + 5O2
یا
6KMnO4 + 9H2SO4 → 9H2O + 3K2SO4 + 6MnSO4 + 5O3
همان طور که می بینید مقدار زیادی آب و اکسیژن(اوزون) تولید می شود، می دانیم واکنش آب با سولفوریک اسید به شدت گرما زا است و گاز اکسیژن هم حجم اشغال می کند( هر مول گاز در صفر درجه سانتی گراد ۲۲/۴ لیتر) بنابر این گاز اکسیژن تولید شده و دمای بالا باعث انفجار شیشه اسید شده است. به علاوه ی این که سولفوریک اسید با پر منگنات، Mn2O7 تولید می کند که نا پایدار است و با انفجار تجزیه می شود.
مطلب مرتبط:




