هیدروژن پلی سولفیدها یا سولفانها (Sulfanes)

تهیه هیدروژن سولفید
بهمن ۲۱, ۱۳۹۶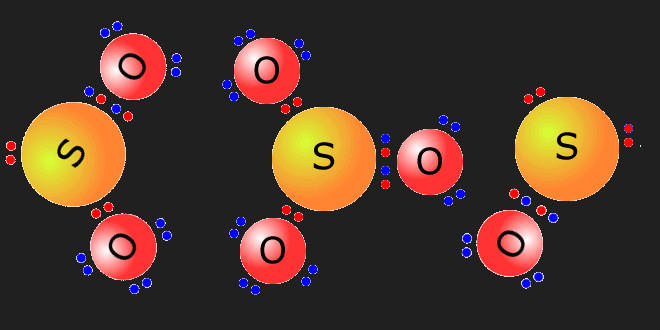
اکسیدها و اسیدهای اکسیژن دار گوگرد(۱)
بهمن ۲۵, ۱۳۹۶گوگرد هم مانند اکسیژن در لایه خارجی خود دارای ۶ الکترون است و مثل آن با برقراری پیوند (پیوند کوئووالانسی یا الکترووالانسی) تعداد الکترونهای لایه خارجی خودش را به ۸ رسانیده و کامل می نماید و بهمان ترتیب که از ترکیب ئیدروژن و اکسیژن دو ترکیب آب H2O و آب اکسیژنه H2O2 بوجود می آید، گوگرد هم که در گروه اکسیژن (از جدول تناوبی) قرار دارد با ئیدروژن ترکیباتی مانند H2S و H2S2 می دهد که بترتیب نظیر H2O و H2O2 می باشند و علاوه بر H2S2 که بنام دی سولفان می باشد گوگرد و ئیدروژن دارای ترکیباتی می باشند که در آنها تعداد گوگردها از سه تا هشت می باشد و بترتیب به آنها تری سولفان (تری هیدروژن سولفید)، تترا سولفان (تترا هیدروژن سولفید)، پنتا سولفان (پنتا هیدروژن سولفید) و …
می گویند و فرمول کلی این ترکیبات بصورت H2Sn می باشد و اتمهای گوگرد پلی سولفورها توسط پیوندهای ساده کوئووالانسی به یکدیگر متصل می باشند یعنی سولفان ها ترکیباتی هستند زنجیری. اگر بجای ئیدروژن پلی سولفورهای ئیدروژن (یعنی بجای ئیدروژن سولفان ها) فلز سدیم قرار گیرد سولفانهای قلیایی تولید میگردد، مثلاً اگر کاتیون بکار رفته در سولفانهای قلیایی کاتیون سدیم باشد ترکیباتی بفرمول زیر بدست خواهد آمد:
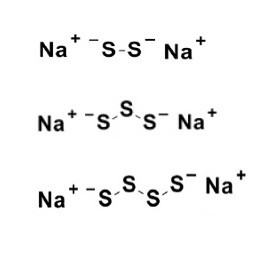
که در آنها یونها به صورت زیر وجود دارد:

هر کدام از یون های
S22- و S32- و S42- و S52-
و … یک آنیون پلی سولفید می باشد و فرمول کلی برای آنها بصورت
Sn2-
می باشد. : همانطوریکه مشاهده می شود در این حالت، پیوندهای میان اتم های گوگرد در
Sn2-
پیوندی ساده و کوئووالانسی دوجانبه است یعنی هر پیوند برقرار شده با به اشتراک گذاشته شدن دو الکترون (که هر الکترون از طرف یک گوگرد است) بوجود آمده است و گوگردهای دو انتهای زنجیر هم هر کدام با گرفتن یک الکترون از فلز (مثلاً فلز قلیایی) ساختمان ناقص خودشان را (یعنی یک الکترون کسری خودشان را) کامل می کنند، تا اینکه آنیون بوجود آید.
پلی سولفورها در محیط اسیدی ناپایدار بوده و تجزیه می شوند و مواد حاصل از تجزیه آنها هیدروژن سولفید و گوگرد می باشد.
هیدروژن پلی سولفید ترکیبی است روغنی شکل که اگر حرارت داده شود تجزیه شده و و گوگرد تولید میکند طبق فرمول زیر:
H2Sn → H2S + Sn-1
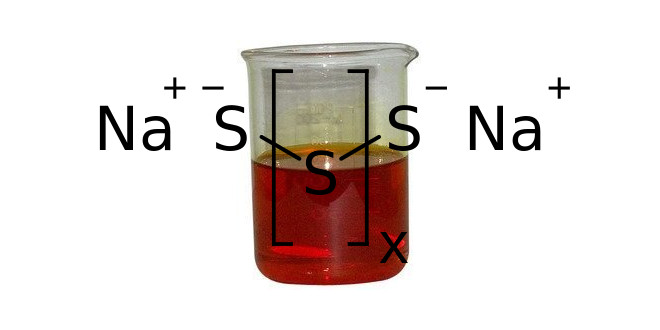
رنگ پلی سولفورها از زرد تا قرمز تیره تغییر می کند و شدت رنگ آنها به تعداد اتم های گوگرد موجود در مولکول آنها بستگی دارد و اگر تعداد اتمهای گوگرد آنها در آنیون سولفیدکم باشد زردرنگ و اگر بیشتر باشد قرمز تیره خواهد بود، بطوریکه روغنی شکل و زردرنگ می باشد.
تری هیدروژن سولفید مایعی زرد کمرنگ با پیوندهای ساده و دارای ساختمانی به شکل زیگزاگ میباشد.
تترا سولفیدسدیم ، پنتا سولفیدسدیم نیز مایعاتی روغنی شکل می باشند.
روش دیگر برای تهیه پلی سولفورهای قلیایی ذوب کردن فلزات قلیایی با گوگرد می باشد و بدین وسیله پلی سولفورهای قلیایی حاصل می شود.
کاربرد سدیم پلی سولفید: ساخت مواد رنگزا و رنگ های گوگردی، حشره کش ها، پلاستیک های مقاوم در برابر روغن، افزودنی های نفتی، آبکاری
دریگر مطالب مرتبط با گوگرد
برای سهولت در بازبینی وب سایت شیمی کیمیکال و ده ها وب سایت شیمی ایرانی و خارجی دیگر و شبکه های اجتماعی مرتبط و همچنین سهولت در به اشتراک گذاری مطالب آن ها اپلیکیشن رایگان کیمیکال پلاس را نصب کنید.





2 Comments
با سلام و تشکر از گرد اورنده این مطالب . بسیار مفید بود
با سلام . مطالب شما بسیار عالی بود . لطفا در صورت امکان منبع این مطالب را برای بنده ایمیل نمایید . با سپاس