فرمول تجربی و مولکولی
چند نوع آب از نظر ایزوتوپی داریم؟
مهر ۲۳, ۱۳۹۶
نکات کنکوری شیمی ۱۶ (غلظت ها)
مهر ۲۶, ۱۳۹۶- kian kiani
- kiandroid.ir
- kimical.ir
- آمادگی کنکور شیمی
- آموزش شیمی
- اپلیکیشن شیمی
- اپلیکیشن های شیمی
- تست شیمی
- تست های شیمی
- تقویتی شیمی
- تمرین های اضافی شیمی
- حا مسائل شیمی یازدهم
- حل تمرین های شیمی دهم
- حل تمرین های شیمی یازدهم
- حل مسائل شیمی دهم
- درس شیمی
- سایت شیمی
- سوالات کنکور شیمی
- شیمی
- شیمی دانشگاهی
- صنایع شیمی
- صنایع شیمیایی
- صنعت شیمی
- فرمول تجربی
- فرمول ساده
- فرمول مولکولی
- کنکور شیمی
- کیان دروید
- کیمیکال
- نکات کنکوری شیمی
- نکته های کنکوری شیمی
- نمونه تمرین های شیمی
- نمونه مسائل شیمی شیمی پیش دانشگاهی
- وب سایت شیمی
ابتدا تعریف فرمول تجربی و مولکولی
ساده ترین نسبت میان اتمهای یک ترکیب را فرمول تجربی یا ساده می گویند.
و نسبت های واقعی اتم ها در ترکیب فرمول مولکولی می گویند
برای نمونه فرمول تجربی آب اکسیژنه HO است و فرمول مولکولی آن H2O2 می باشد.
برای تعیین فرمول تجربی مراحل زیر را باید انجام دهید
۱- ابتدا مقادیر داده شده را که بر حسب درصد یا گرم یا میلی گرم است را تقسیم بر جرم اتمی هر عنصر می کنیم تا اتم گرم(مول) هر یک به دست آید.
۲- اتم گرم های به دست آمده را تقسیم بر کوچک ترین عدد می کنیم تا نسبت فرمول تجربی به دست آید
۳- برای به دست آوردن فرمول مولکولی باید فرمول تجربی را در n ضرب کنیم و آن را برابر جرم مولکولی قرار دهیم تا n به دست آید سپس عدد n را در فرمول تجربی ضرب می کنیم تا فرمول مولکولی به دست آید.
یک تست شیمی عمومی:
– ۶۰٪ از یکی از اکسیدهای عنصر X به جرم اتمی ۳۲ را اکسیژن تشکیل می دهد. ساده ترین فرمول ممکن برای این اکسید کدام است؟(O=16)
1) XO2
2) XO3
3) X2O3
4) XO
– یک مولکول با وزن مولکولی ۱۸۰/۱۸ گرم بر مول تجزیه شده و شامل ۴۰٪ کربن، ۶/۷۲٪ هیدروژن و ۵۳/۲۸٪ اکسیژن است. فرمول تجربی و فرمول مولکولی آن کدام است؟
فرمول مولکولی C6H12O6 می باشد.
گاهی به جای آن که جرم مولکولی را مستقیم بدهند چگالی یا چگالی نسبی را می دهند که در این صورت ابتدا باید جرم مولکولی را حساب کرد:
چگالی:
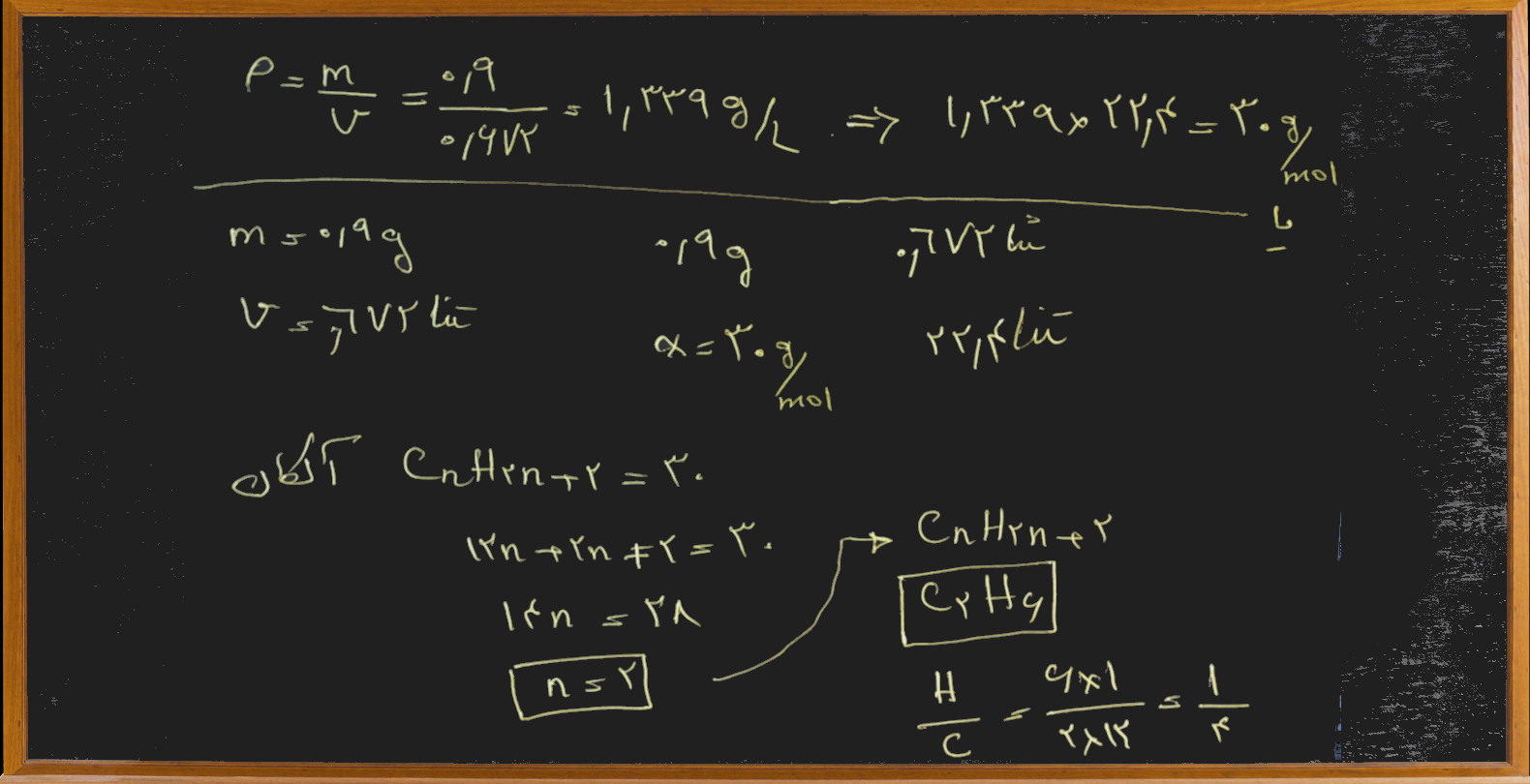
- اگر در شرایط متعارفی، ۰/۹ گرم از یک آلکان گازی ۰/۶۷۲ لیتر حجم داشته باشد نسبت جرم هیدروژن به کربن در مولکول آن کدام است؟
به منظور فراگیری انواع محاسبات شیمی آلی اپلیکیشن اندرویدی شیمی آلی را نصب کنید و بخوانید
برای سهولت در بازبینی وب سایت شیمی کیمیکال و ده ها وب سایت شیمی ایرانی و خارجی دیگر و شبکه های اجتماعی مرتبط و همچنین سهولت در به اشتراک گذاری مطالب آن ها اپلیکیشن رایگان کیمیکال پلاس را نصب کنید.

سرچشمه ها:
https://www.thoughtco.com/calculate-empirical-and-molecular-formula-609503

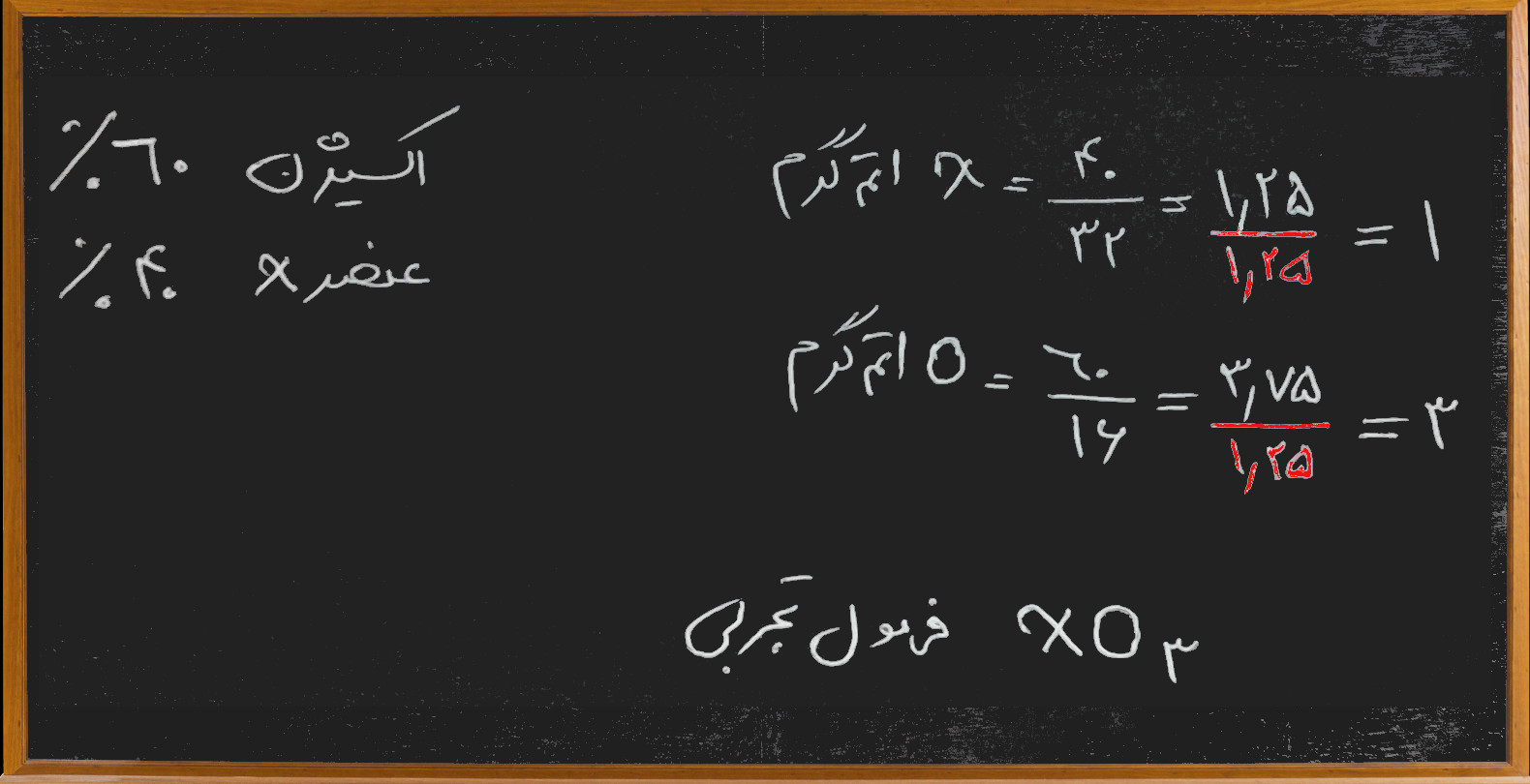
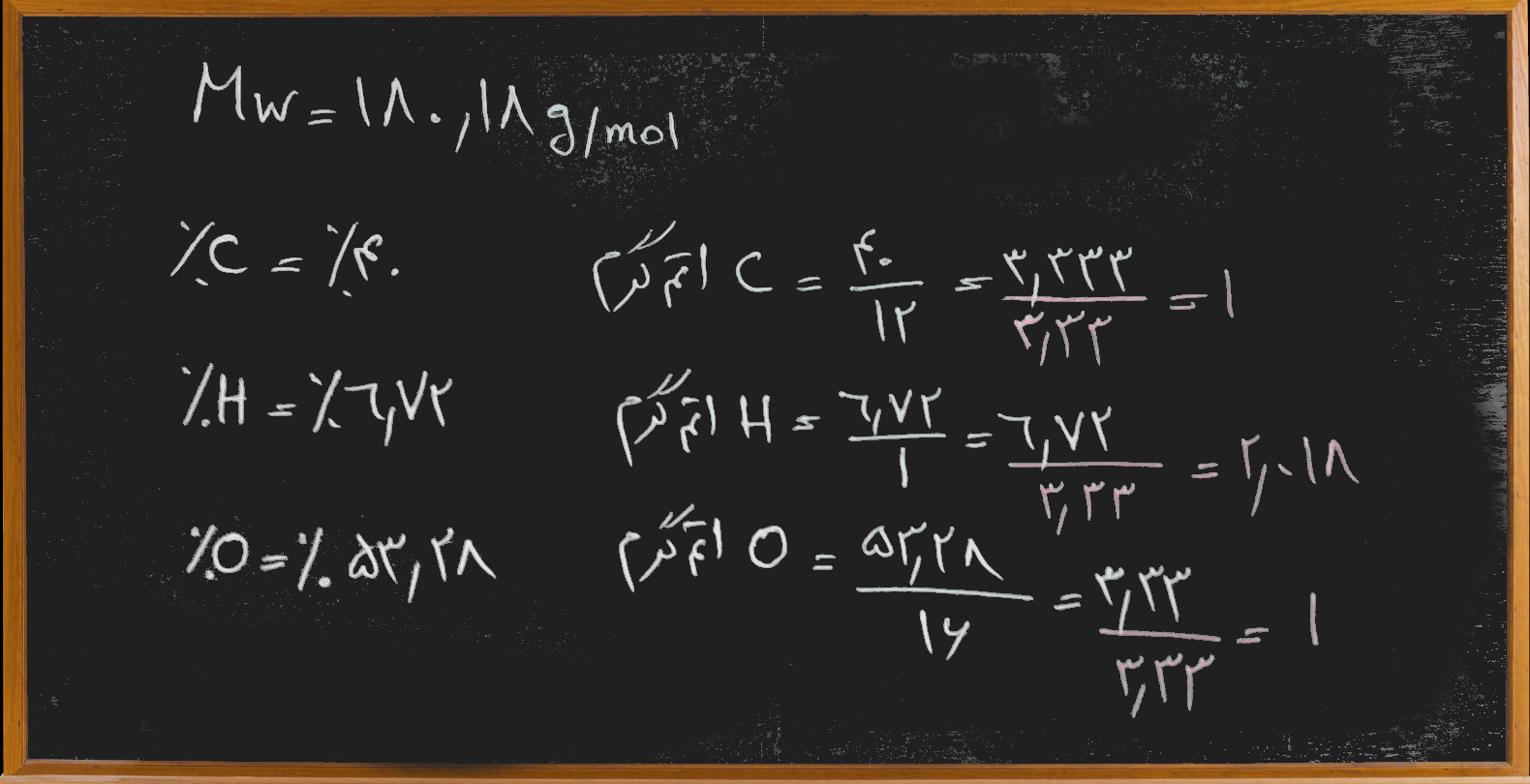
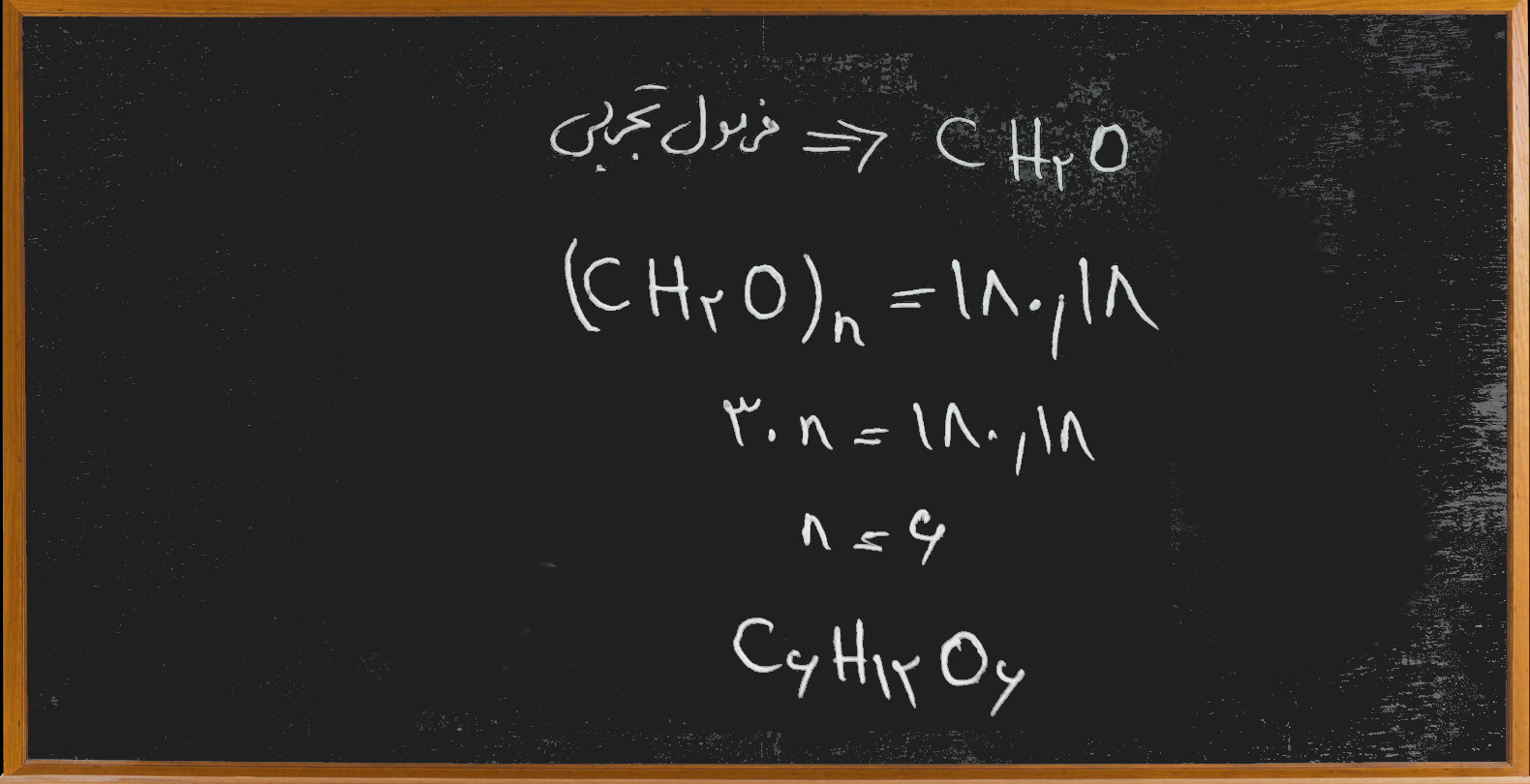



2 Comments
می شه لطفا برعکسشم بنویسید؟
نه