عناصر برای کودکان(برلیوم)

نرم افزار ChemDraw (بخش سوم)
مرداد ۲۱, ۱۳۹۸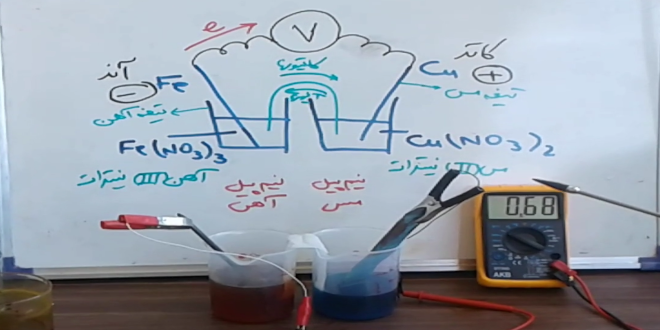
پیل الکتروشیمیایی (آهن-مس)
مهر ۱۴, ۱۳۹۸برلیوم
Be: نماد
عدد اتمی :4
جرم اتمی:9.0122
گروه : فلزات قلیایی خاکی
حالت در دمای اتاق: جامد
چگالی<دانسیته>: 1.85 گرم بر سانتی متر مکعب
1287C , 2349Fنقطه ذوب :
2469 C , 4476 F نقطه جوش:
کشف شده توسط لوییس نیکولاس درسال 1798 میلادی
برلیوم یک فلز خیلی کمیاب است که تقریبا هرگز در حالت خالص قابل یافتن نیست و جزو گروه فلزات قلیایی خاکی است که دومین ستون از جدول تناوبی را تشکیل می دهد.
خصوصیات و ویژگی ها
در حالت آزاد برلیوم فلزی سخت و در عین حال ترد و شکننده است. همچنین رنگ آن به صورت نقره ای <خاکستری> فلزی است.
برلیوم بسیار سبک وزن است و در عین حال یکی از بالاترین نقطه های ذوب را در بین تمامی عناصر سبک فلزی دارد.برلیوم فلزی مغناطیسی نیست< به این معنا که توسط آهنربا جذب ویا دفع نمی شود> و خاصیت هدایت گرمایی بالایی دارد.
برلیوم جزو مواد سرطان زا به حساب می آید به این معنا که میتواند در انسان باعث بروز سرطان شود . همچنین برلیوم ماده ای سمی برای انسان به حساب می آید و باید با احتیاط و رعایت نکات ایمنی لمس شود < استفاده از دستکش و با رعایت موارد ایمنی >و توجه داشته باشید که هرگز برلیوم را مزه نکنید و از بلعیدن آن خودداری کنید.
برلیوم در کجای زمین یافت می شود؟
برلیوم اغلب اوقات در بریل <سیلیکات برلیوم آلمینیوم >های معدنی یافت میشود . برلیوم در پوسته زمین و اغلب در سنگ های آتشفشانی یافت میشود.
اکثر برلیوم جهان حاصل استخراج از معادن ایالات متحده آمریکا ایالت یوتا و روسیه تهیه میشود که تقریبا دو سوم از محصول برلیوم کل جهان است .
برلیوم همچنین در سنگ های گران بها مانند زمرد و زمرد کبود قابل یافتن است.
برلیوم امروزه چگونه مورد استفاده قرار می گیرد؟
برلیوم کاربرد های زیادی دارد . بسیاری از کاربرد های این ماده در تکنولوژی های پیشرفته و کاربرد های نظامی است .یکی از کاربرد ها در پنجره ماشین های اشعه اکس است. برلیوم بصورت طبیعی <ذاتی> دارای توانایی خاص برای ظاهر و آشکار کردن اشعه های ایکس دارد. استفاده دیگر برلیوم به عنوان مهارگر و یا سپری < سپر ایمنی >در راکتور های هسته ای است.
برلیوم همچنین برای ساخت آلیاژ ها مانند برلیوم مس و برلیوم نیکل کاربرد دارد که این آلیاژ ها برای ساخت لوازم پزشکی و ابزار های ظریف و و ابزارهای ضد جرقه ای که در نزدیکی گازهای قابل اشتعال استفاده میشوند کاربرد دارد.
برلیوم چگونه کشف شد؟
درسال 1798 میلادی شیمیدان فرانسوی لوییس نیکولاس در خاستی مبنی بر تجزیه و تحلیل زمرد و بریل <سیلیکات برلیوم آلمینیوم> بهمراه معدن شناس رن هاوی اراعه داد. در حین تجزیه و تحلیل ماده / لوییس ماده جدیدی در هردوی آنها کشف کرد. او در آغاز به آن ماده نوعی زمین جدید می گفت و به زودی آن ماده را بخاطر طعم شیرینش گلاسینیوم نامگذاری کردند < نکته : هرگز آن را مزه نکنید چون ماده ای بسیار سمی است>.
نام برلیوم از کجا آمده است؟
در سال 1828 میلادی اولین برلیوم خالص بوسیله شیمیدان آلمانی فرندریچ ولر جداسازی شد . او نام گلاسینیوم که را برای عنصر دوست نداشت به همین خاطر نام آن را به برلیوم تغیر داد که به معنای < از بریل معدنی > است.
ایزوتوپ ها:
12 ایزوتوپ شناخته شده برای برلیوم موجود است . اما فقط یکی از آنها پایدار است . برلیوم ده هنگامی تولید میشود که اشعه های عظیم <خورشید> به اکسیژن اتمسفر برخورد می کنند.
حقایق جالب در مورد برلیوم
• لوییس نیکولاس همچنین عنصر کرومیوم را هم کشف کرده است.
• یک اتم برلیوم دارای چهار الکترون و چهار پروتون است.
• برلیوم در آغاز بصورت ترکیبی با اکسیژن کشف شد که به آن برلیوم اکسید گفته می شد.
• آلیاژ های برلیوم میتوانند فلزهای سخت/ محکم / و با وزن کم تولید کند که در فضاپیماها/ موشک ها / ماهواره ها / و هواپیما های سرعت بالا <جت ها> مورد استفاده قرار می گیرند.
• قرار گرفتن زیاد در برابر برلیوم میتواند موجب مشکلات و بیماری های تنفسی < ریه > شود که به آن برلیوزیس < BERYLLIOSIS > گفته می شود.
سرچشمه:
https://www.ducksters.com/science/chemistry/beryllium.php
برگردان به پارسی: رضا زمانی




